转自:蚌埠新闻网
近日,中国生物制药(1177.HK)传来振奋人心的消息,其1类创新药ROCK2抑制剂TDI01混悬液被国家药品监督管理局药品审评中心(CDE)纳入突破性治疗药物程序(BTD),用于治疗既往经过1线不超过5线系统治疗的中重度慢性移植物抗宿主病(cGVHD)。这一消息无疑为相关患者带来了新的希望,也彰显了中国生物制药在创新药物研发领域的雄厚实力。
cGVHD作为异基因造血干细胞移植(allo-HSCT)后的主要并发症之一,严重威胁着患者的健康。其发生率处于30-70%的高位,在存活超过5年的患者中,cGVHD的发病率更是超过50%,超一半的患者需要在2年内接受二线治疗。而且,该并发症是导致非复发死亡率(NRM)的常见原因之一。一项回顾性单中心分析研究指出,非典型cGVHD的表现是NRM的主要原因,其中37.8%的NRM与cGVHD有关。在此背景下,TDI01混悬液的出现意义非凡。
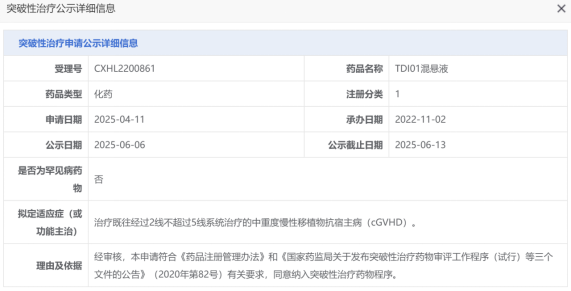
TDI01混悬液作为一种创新、口服、高选择性ROCK2抑制剂,是国内首个自主研发的ROCK2抑制剂。它具有独特的作用机制,一方面能够有效抑制促炎性Th17细胞,促进调节性T细胞,进而恢复免疫稳态;另一方面,ROCK2抑制剂直接作用于成纤维细胞的ROCK2靶点,阻断成纤维细胞分化成肌成纤维细胞,并诱导已存在的肌成纤维细胞凋亡,实现免疫稳态并逆转纤维化的双重机制。
在第51届欧洲血液与骨髓移植学会年会(EBMT2025)上,北京大学人民医院莫晓冬教授在总统专场环节(GS2PresidentialSymposium)口头报告了“TDI01用于中重度慢性移植物抗宿主病治疗的Ib/II期研究结果”。结果显示,在经过1-5线既往治疗的中重度cGVHD患者中,TDI01显示出有前景的有效性和可接受的安全性,这无疑为cGVHD的治疗开辟了新的路径。
值得一提的是,此前TDI01已在国内获批开展特发性肺纤维化、尘肺病、肝纤维化的临床试验。中国生物制药凭借不断地创新和努力,在医药研发的道路上持续前行,其研发的TDI01正逐步展现出巨大的潜力,有望为更多患者带来福音,推动相关疾病治疗领域的发展。随着TDI01在临床研究中的不断推进,我们有理由期待中国生物制药将为全球患者带来更多创新的治疗方案。
[广告]免责声明:本内容为广告,相关素材由广告主提供,广告主对本广告内容的真实性负责。蚌埠新闻网登载此文出于传递更多信息之目的,并不意味着赞同其观点或证实其描述。文章内容仅供参考,不构成投资、消费建议。据此操作,风险自担!!!
转自:滚动播报