
Rapid and sensitive detection of staphylococcal enterotoxin E using a time resolved fuorescence immunochromatography assay
第一作者:南黎
通信作者:温凯
研究背景
葡萄球菌食物中毒是一种常见的食源性疾病,主要由金黄色葡萄球菌产生的葡萄球菌肠毒素引起。据报道,乳制品中葡萄球菌肠毒素E(Staphylococcal enterotoxin E,SEE)污染事件频发,令人堪忧的是,婴儿配方奶粉中曾发现存在SEE,对婴幼儿的健康构成重大隐患。因此,定期筛查婴儿配方奶粉中的SEE,对于确保食品安全和严格控制质量标准至关重要。
目前,食品中毒素检测的首选方法是免疫分析法,如酶联免疫吸附测定(Enzyme linked immunosorbent assay,ELISA)和侧向流免疫层析分析法(Lateral flow immunochromatographic assay,LFIA)等。然而,这些方法尚不能快速现场定量地检测婴儿配方奶粉中的SEE污染。幸运的是,时间分辨荧光免疫层析分析法(Time-resolved fluorescence immunochromatography assay,TRFICA)促进了快速、现场点对点监测和诊断技术的发展,使其有潜力成为快速、定量检测婴儿配方奶粉中SEE的新方法。本研究设计了一种新型TRFICA用于SEE检测,并与目前广泛使用并被认为是基于免疫分析的金标准的双抗体夹心ELISA(Double antibody sandwich ELISA,DAS-ELISA)方法进行了比较。
全文速览
(1)重组SEE蛋白表达和抗SEE抗体的筛选与表征
纯化后的SEE蛋白分子量为27~34 kDa,与理论分子量一致,且未出现非特异性条带。SDS-PAGE分析显示,重组SEE蛋白的纯度超过90%。从免疫小鼠中制备的8种单克隆抗体(Monoclonal antibodies,mAbs)显示出特征性的50kDa(重链)和25kDa(轻链)条带,其中mAb 9A2对SEE的亲和力最高(IC50 = 41.152 ng/mL),而多克隆抗体(Polyclonal antibody,pAb)对SEE的亲和力最低(IC50 = 125 ng/mL)(图 1)。

图1 重组SEE蛋白的构建示意图
A:SEE-pETt28a示意图;B:纯化后的重组 SEE蛋白的SDS-PAGE分析(M:分子量标记;1:结合层;2~5:分别用30、80、120和500 mmol/L咪唑洗脱的SEE蛋白)
(2)检测SEE的DAS-ELISA方法的建立和优化
当mAb 1A5与pAb配对时,获得了最大的阳性/阴性(Maximum positive/negative,P/N)值。以P/N值为指标最终优化的DAS-ELISA方法:pAb浓度为2.5 μg/mL,mAb浓度为0.5 μg/mL,稀释比为1∶1 000,37 ℃下包被2 h,2%脱脂牛奶封闭,抗原反应时间为60 min,检测抗体反应时间为30 min,HRP标记链霉亲和素稀释比为1∶3 000(图 2)。

图2 DAS-ELISA反应条件的优化
A:配对抗体选择;B:优化pAb浓度;C:优化mAb稀释比例;D:优化包被条件;E:封闭剂选择;F:优化抗原反应时间;G:优化检测抗体反应时间;H:优化HRP标记的链霉亲和素的稀释比例;选择最大P/N值作为最佳反应条件;P/N>2.1表示阳性结果
(3)检测SEE的TRFICA方法的建立和优化
TRFICA能够达到所需荧光水平的条件:pAb体积为16 µL(5.67 mg/mL),mAb为2倍稀释,样品垫材料为玻璃纤维SB08,样品体积为100 µL,反应时间为8 min(图 3)。
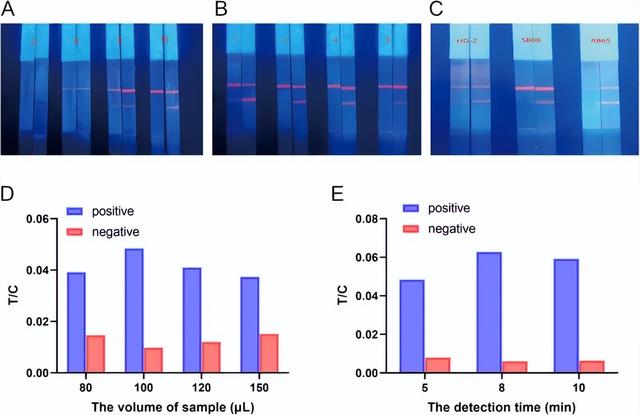
图3 TRFICA反应条件的优化
A:检测抗体用量的优化;B:包被mAb稀释比的优化;C:样品垫材料的选择;D:样品体积的优化;E:检测时间的优化;T/C是测试线(T线)信号强度与控制线(C线)信号强度的比值;下图同
① 灵敏度
TRFICA的SEE标准曲线在0.5~64 ng/mL范围内呈线性(y= 0.010 08x+ 0.020 5,r²= 0.997 8),而DAS-ELISA的SEE标准曲线的线性范围为0.2~3.2 ng/mL,r²为0.998;虽然TRFICA的检测限(0.081 ng/mL)略高于DAS-ELISA(0.028 ng/mL),但TRFICA的检测范围显著宽于DAS-ELISA(图 4)。结果表明,与DAS-ELISA相比,TRFICA不仅保持了相似的灵敏度,还具有更广泛的检测范围和更强的适应性。

图4 SEE的标准曲线
A:DAS-ELISA标准曲线;B:TRFICA标准曲线;C:TRFICA荧光图
② 特异性
结果显示,在肠毒素浓度为100 ng/mL的条件下,使用DAS-ELISA方法时,在SEE和葡萄球菌肠毒素D(Staphylococcal enterotoxin E,SED)之间存在1%的交叉反应率;然而,在使用TRFICA方法时,未观察到与其他对比抗原存在交叉反应(图 5)。结果表明,TRFICA在检测SEE方面具有更高的特异性。
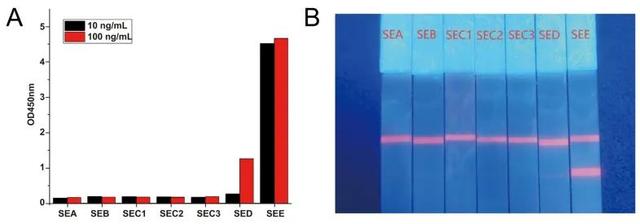
图5 DAS-ELISA(A)和TRFICA(B)与不同葡萄球菌肠毒素血清型之间的交叉反应率(TRFICA交叉反应肠毒素的浓度为100 ng/mL)SEA:葡萄球菌肠毒素A;SEB:葡萄球菌肠毒素B;SEC1:葡萄球菌肠毒素C1;SEC2:葡萄球菌肠毒素C2;SEC3:葡萄球菌肠毒素C3;SED:葡萄球菌肠毒素D;SEE:葡萄球菌肠毒素E;表2同
③ 准确度和精密度
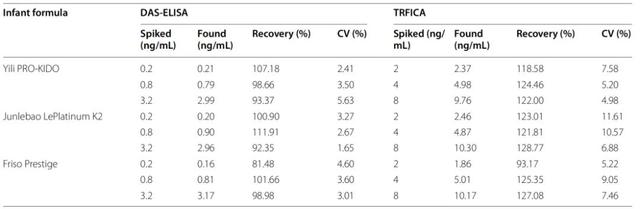
结果显示,TRFICA在婴儿配方奶粉中的回收率范围为93.17%~128.77%,精密度小于12%;而DAS-ELISA的回收率范围为81.48%~111.91%,精密度小于6%(表 1)。结果表明,这2种方法均可准确检测奶粉中的SEE。
表1 DAS-ELISA和TRFICA对婴儿配方奶粉中SEE的回收率
(4)不同SEE检测方法的比较
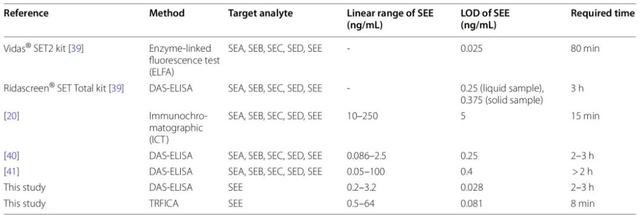
SEE检测的免疫分析法通常多集中于同时检测5种经典葡萄球菌肠毒素(表 2)。本研究解决了快速识别SEE方法的迫切需求,建立了针对SEE的灵敏且个体化检测方法。本研究开发的TRFICA和DAS-ELISA方法在SEE的检测限上优于文献报道的方法,并与商业Vidas® SET2试剂盒相当。TRFICA方法结合了荧光分析和LFIA的优点,其灵敏度与ELISA相当,且优于传统的LFIA。此外,TRFICA还显著缩短了反应时间,使其成为单一样品或多样品同时检测的更简便、更灵活的选择。
表2 已发表的SEE检测方法的比较
编辑荐语
本研究开发的时间分辨荧光免疫层析分析法结合了荧光分析和侧流免疫层析技术,达到了与ELISA方法相当的灵敏度,同时提高了检测方法的简便性和灵活性,缩短了反应时间,为婴儿配方奶粉中葡萄球菌肠毒素E的现场检测提供了宝贵的解决方案。
作者介绍

第一作者:南黎
中国农业大学动物医学院,2021级博士研究生。研究方向为动物源性食品安全。

通信作者:温凯
中国农业大学,博士生导师。主要从事动物源性食品安全检测和动物疫病诊断相关研究,涉及抗体、受体、核酸等生物识别材料制备技术、进化改造技术以及快速检测技术和产品研发。主持和参与国家及省部级项目10项、制订或修订国家及行业标准项目4项,在Analytical Chemistry、Analytica Chimica Acta、Sensors and Actuators B等国际期刊上以第一作者/通信作者(含共同)发表SCI论文15篇,申请国家发明专利28项,获授权15项。研制的快速检测产品通过转化合作获得北京市新技术新产品证书6项、改良型新兽药兽用诊断制品1项,获得2015年“国家技术发明奖二等奖”、2021年“第十二届大北农科技奖一等奖”、2021年“北京市科学技术进步奖二等奖”、2023年“第九届中国国际“互联网+”大学生创新创业大赛北京赛区一等奖”。
原文链接
Li, N., Xie, JQ., Li, Q. et al. Rapid and sensitive detection of staphylococcal enterotoxin E using a timeresolved fuorescence immunochromatography assayOne Health Adv.2, 28 (2024).https://onehealthadv.biomedcentral.com/articles/10.1186/s44280-024-00063-x
