9月27日,Poseida Therapeutics宣布了P-BCMA-ALLO1在复发/难治性多发性骨髓瘤(RRMM)患者中的1期试验的新中期临床数据。

截图来源于参考资料1,侵权请联系删除
P-BCMA-ALLO1是一款同种异体CAR-T 细胞疗法,用于治疗多发性骨髓瘤(MM)。共72例患者纳入意向治疗人群,结果显示:客观缓解率(ORR)为54%,其中,11%的患者实现完全缓解(CR)或严格完全缓解(sCR),33%的患者实现非常好的部分缓解或更高(VGPR+)。

截图来源于参考资料2,侵权请联系删除
队列C的23例患者客观缓解率(ORR)高达91%,既往未接受过BCMA靶向治疗患者的客观缓解率(ORR)高达100%,既往至少接受过一次靶向BCMA治疗和/或talquetamab的患者客观缓解率(ORR)为86%。完全缓解率(CR)或严格完全缓解率(sCR)为22%,非常好的部分缓解或更高缓解率(VGPR+)为48%。

截图来源于参考资料2,侵权请联系删除
该试验中1例71岁女性患者,伴有肝脏,乳房和淋巴结转移,BCMA-ALLO1治疗后第五个月就实现了非常好的部分缓解或更高(VGPR+)。
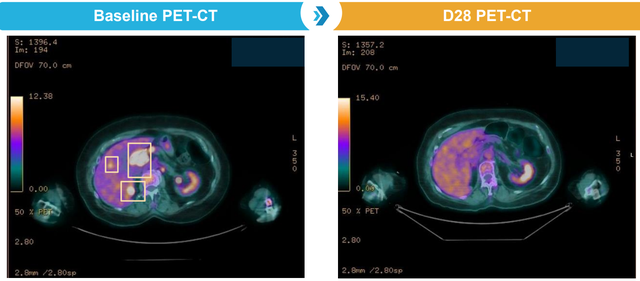
截图来源于参考资料2,侵权请联系删除
另1例59岁男性患者在BCMA-ALLO1治疗后实现持续性的部分缓解(PR)。
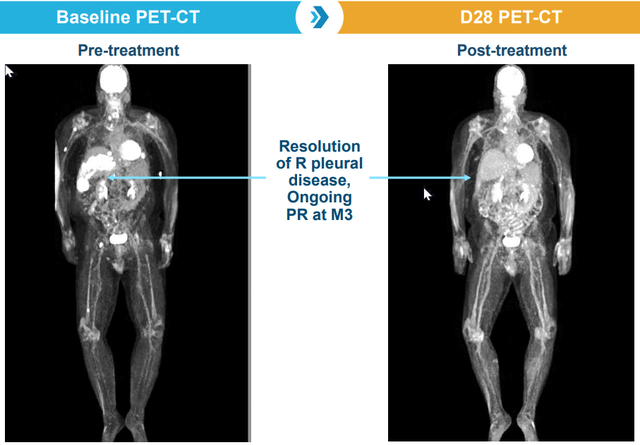
截图来源于参考资料2,侵权请联系删除
该试验表明,BCMA-ALLO1治疗多发性骨髓瘤患者具有显著疗效。
多发性骨髓瘤(MM)是血液系统的常见恶性肿瘤,被称为“吃骨头”的血液病。目前我国多发性骨髓瘤发病率正逐年上升,严重危害公众健康。CAR-T细胞疗法作为肿瘤治疗的“重要杀伤武器”,目前已经在多发性骨髓瘤中取得鼓舞成就。
CAR-T细胞疗法GC012F治疗多发性骨髓瘤
7月25日,《美国医学会杂志》(JAMA)发表了BCMA/CD19 双靶向CAR-T细胞疗法GC012F在高危新诊断多发性骨髓瘤患者中的疗效。

图片来源于参考资料3,侵权请联系删除
在19例患者中评估疗效,客观缓解率(ORR)高达100%,也就是说所有患者均出现不同程度的肿瘤反应,最佳反应为所有患者出现严格意义的完全缓解(sCR)状态,第一次严格完全缓解的中位时间为84天。
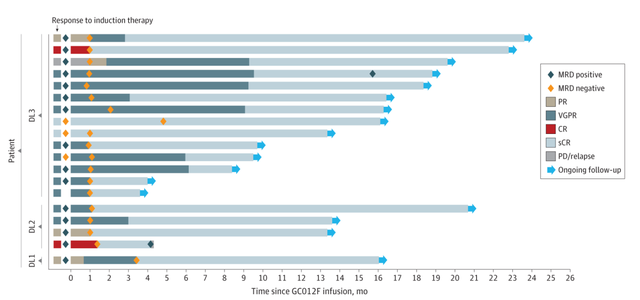
图片来源于参考资料3,侵权请联系删除
结果表明,GC012F在高危新诊断多发性骨髓瘤患者中可能是一种安全的治疗方法。
CAR-T细胞疗法PHE885治疗多发性骨髓瘤
在2024年国际骨髓瘤学会年会上公布了Durcabtagene autoleucel (PHE885)在复发/难治性(R/R)多发性骨髓瘤患者中的II期研究(NCT05172596)结果。

截图来源于参考资料4,侵权请联系删除
Durcabtagene autoleucel(PHE885)是一款靶向BCMA的CAR-T细胞产品,该试验共145例患者接受治疗,结果显示:客观缓解率(ORR)为97%,临床反应率(CRR)为 53%,半年无进展生存率(PFS)为86%。在接受10e6细胞剂量治疗且随访至少6个月的患者中,客观缓解率(ORR)为92%,临床反应率(CRR)为53%,半年无进展生存率(PFS)为82%。
试验表明,PHE885在复发/难治性多发性骨髓瘤患者中具有较高反应。
结语
嵌合抗原受体T(CAR-T)细胞疗法是医学界的研究热点,通过从患者身上分离出T细胞,经过工程改造升级来杀死肿瘤细胞。目前CAR-T细胞已在多发性骨髓瘤、急性淋巴细胞白血病等血液肿瘤,胃癌、脑胶质瘤、前列腺癌、乳腺癌、卵巢癌、肝癌等实体瘤以及红斑狼疮等自身免疫系统疾病方面取得突破性的进展。目前定价较高,均在百万以上。不过研究人员正在积极带领CAR-T走向大众,相信未来会有更多患者用的起CAR-T细胞疗法,并成功从中获益。
参考资料
1.https://investors.poseida.com/news-releases/news-release-details/poseida-therapeutics-reports-positive-interim-phase-1-results
2.https://investors.poseida.com/static-files/636a7f34-056c-4a4e-ba58-25f8d0a16dc6
3.https://jamanetwork.com/journals/jamaoncology/fullarticle/2821602#google_vignette
4.https://imsannual2024.eventscribe.net/fsPopup.asp?PresentationID=1496711&returl=YWpheGNhbGxzL3Nlc3Npb25pbmZvLmFzcD9QcmVzZW50YXRpb25JRD0xNDkzODA5&mode=presinfo
免责声明:文本参考来源于网络,版权归原作者所有。
该文章仅供分享,如涉嫌侵犯您的著作权请联系我们删除,谢谢!