【CMT&CHTV 文献精粹】
导语:肾透明细胞癌(ccRCC)是一种恶性程度较高的肿瘤,其发病机制复杂,与VHL基因的突变和HIF-2α信号通路的异常激活紧密相关。近年来,尽管针对HIF-2α的抑制剂如Belzutifan已获得FDA批准用于治疗VHL相关肿瘤,但治疗响应率不高,且易产生耐药。最新研究进展表明,代谢酶ACSS2在ccRCC中扮演着关键角色。ACSS2,即乙酰辅酶A合成酶2,负责将乙酰盐转化为乙酰辅酶A,是细胞代谢过程中的重要酶。在ccRCC中,ACSS2的表达与患者预后不良相关,但其在肿瘤生长和HIF-2α信号传导中的具体作用尚不明确。
2024年6月,《The Journal of Clinical Investigation》发表题为“HIF-2α expression and metabolic signaling require ACSS2 in clear cell renal cell carcinoma”的文章,探索ACSS2在ccRCC中的作用机制,以及其作为治疗靶点的潜力,揭示了ACSS2在ccRCC中的多重作用机制。

研究方法概述
该研究采用了多种实验方法来探究ACSS2在透明细胞肾癌(ccRCC)中的作用及其对HIF-2α信号通路的影响。以下是研究方法的概述:
体外实验:
细胞培养:使用了ccRCC细胞系(如786-O和A498)进行实验。
ACSS2抑制:通过使用药理学抑制剂(ACSS2i)或转导含有shRNA的病毒载体来降低ACSS2的表达。
细胞增殖和生长评估:采用BrdU掺入实验和晶体紫染色来评估细胞增殖和生长情况。
肿瘤球形成实验:评估ACSS2抑制对肿瘤细胞形成肿瘤球能力的影响。
体内实验:
动物模型:使用NOD scid IL2Rgnull (NSG)小鼠进行肿瘤异种移植模型实验。
肿瘤形成和治疗:将ccRCC细胞注射到小鼠体内,然后通过口服或腹腔注射给予ACSS2抑制剂。
分子生物学技术:
蛋白质提取和西方印迹分析(Western blot):用于检测HIF-2α和其他相关蛋白的表达水平。
免疫沉淀:用于研究MUL1与HIF-2α之间的相互作用。
免疫组织化学和免疫荧光:用于分析ACSS2和HIF-2α在组织样本中的表达和定位。
基因表达分析:
ATAC-seq:用于分析ACSS2抑制对染色质可及性的影响。
NanoString nCounter Metabolic Pathways panel:用于评估ACSS2抑制对代谢途径相关基因表达的影响。
代谢分析:气相色谱-质谱联用技术(GC-MS):用于定量分析胆固醇和其他脂质。
形态学分析:透射电子显微镜(TEM):用于观察ACSS2抑制对线粒体形态的影响。
功能性分析:Mitochondrial biogenesis assay:用于评估ACSS2对线粒体生物合成的影响。
研究结果
ACSS2在ccRCC中的作用
研究首先揭示了ACSS2在ccRCC中的重要作用。通过在786-O和A498细胞系中使用ACSS2抑制剂(ACSS2i)或shACSS2,观察到HIF-2α水平的显著降低,同时抑制了体外细胞生长。具体数据显示,在24小时处理后,所有剂量的ACSS2i均显著减少了BrdU掺入,表明ccRCC细胞系的增殖能力受到了抑制。此外,3D肿瘤球形成实验也表明ACSS2i处理显著降低了肿瘤球的形成能力。

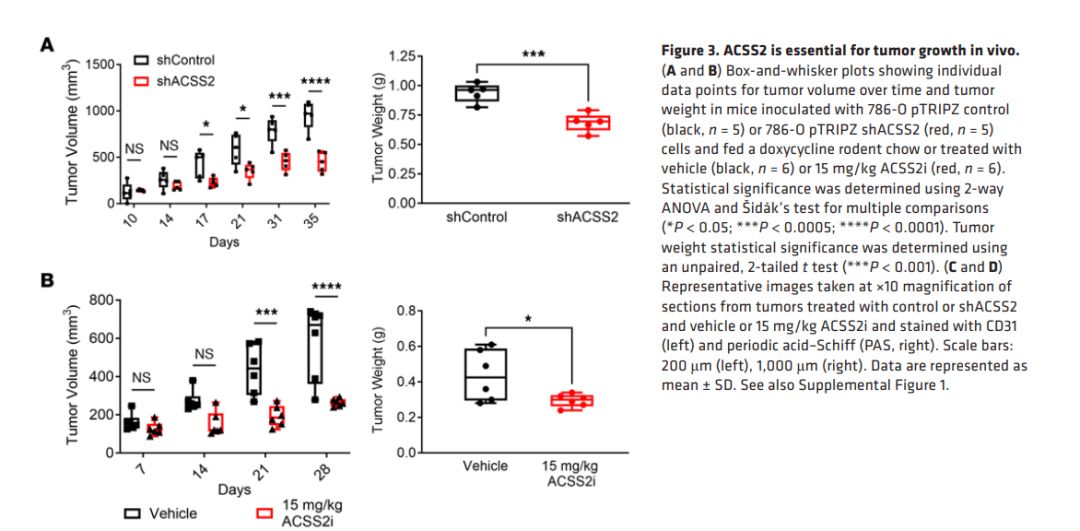
ACSS2抑制对肿瘤生长的影响
在体内模型中,通过给予小鼠ACSS2i或通过诱导shACSS2表达,观察到肿瘤生长和最终肿瘤重量的显著减少。通过给予15 mg/kg ACSS2i处理的小鼠,其肿瘤体积和重量均显著小于对照组(P < 0.05; P < 0.0005; P < 0.0001;P < 0.001),这表明ACSS2在肿瘤生长中起着关键作用。

ACSS2对HIF-2α稳定性的调控
研究进一步探讨了ACSS2对HIF-2α稳定性的影响。通过使用蛋白酶体抑制剂MG132预处理细胞,发现在ACSS2抑制后,HIF-2α的表达得到了显著恢复,这表明ACSS2可能通过促进HIF-2α的蛋白酶体降解来降低其稳定性。此外,ACSS2i处理还导致自噬和蛋白酶体途径的激活,这可能进一步促进了HIF-2α的降解。

MUL1与HIF-2α的相互作用
研究还发现了一个新的调控HIF-2α稳定性的机制,即E3泛素连接酶MUL1与HIF-2α的相互作用。通过免疫共沉淀实验,证实了MUL1与HIF-2α的结合,并发现ACSS2抑制剂处理并不影响这一相互作用。此外,MUL1的过表达能够降低HIF-2α蛋白水平,并减少HIF-2α下游靶基因的表达。
ACSS2对代谢途径的影响
ACSS2的抑制对ccRCC细胞的代谢途径产生了广泛影响。通过NanoString代谢途径检测和ATAC-seq分析,发现ACSS2抑制导致胆固醇代谢途径的显著变化,以及染色质可及性的减少。这些结果表明,ACSS2促进HIF-2α的转录和蛋白质表达,还可能通过改变代谢途径和染色质状态来影响ccRCC细胞的表型。且ACSS2对ccRCC生长和HIF-2α信号传导的调节直接依赖于ACSS2酶活性。
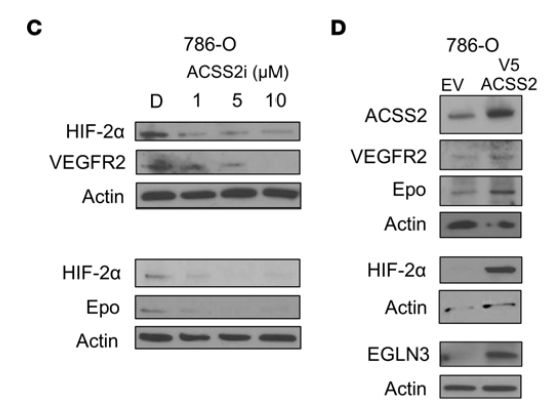
ACSS2酶活性对肿瘤生长的影响
研究最后探讨了ACSS2酶活性对肿瘤生长的影响。通过使用催化失活的ACSS2突变体(ΔT376K),发现只有野生型ACSS2(WT-ACSS2)能够恢复因ACSS2缺失导致的HIF-2α表达下降和细胞生长抑制,而ΔT376K则无法完全恢复。这表明ACSS2的酶活性对于维持ccRCC细胞的HIF-2α表达和促进肿瘤生长至关重要。
总结讨论
研究揭示了ACSS2在ccRCC中的多重作用机制。ACSS2的抑制不仅能够降低HIF-2α水平,还能够影响肿瘤细胞的代谢途径和染色质状态。特别是,ACSS2与MUL1相互作用的发现,对于HIF-2α稳定性的调控有了新的了解,可能有助于开发针对HIF-2α的新药物。此外,ACSS2抑制剂在体外和体内模型中均显示出对ccRCC生长的抑制作用,这为未来的临床试验提供了有力的前期数据。考虑到HIF-2α在ccRCC中的中心作用,ACSS2抑制剂可能成为一种有效的治疗手段,尤其对于VHL突变的ccRCC患者。这些发现对基础科学研究具有重要意义,也有望改善ccRCC患者的预后。
参考文献:
Bacigalupa ZA, Arner EN, Vlach LM, et al. HIF-2α expression and metabolic signaling require ACSS2 in clear cell renal cell carcinoma[J]. J Clin Invest. 2024;134(12):e164249. Published 2024 Jun 17. doi:10.1172/JCI164249
“医学论坛网”发布医学领域研究成果和解读,供专业人员科研参考,不作为诊疗标准,使用需根据具体情况评估。
编辑:且行
二审:清扬
三审:碧泉
排版:半夏