近日,Wugen宣布同种异体靶向CD7 靶向 CAR-T 细胞疗法WU-CART-007的关键试验中实现首批患者给药。

WU-CART-007是一种潜在的同类首创、在研抗 CD7 CAR-T 细胞疗法,用于治疗复发或难治性(R/R)T 细胞急性淋巴细胞白血病或 T 细胞儿童和成人患者细胞淋巴母细胞淋巴瘤(T-ALL/LBL)。2024年美国血液学会(ASH)年会上报告了WU-CART-007用于复发/难治性(R/R) T 细胞急性淋巴细胞白血病/淋巴瘤(T-ALL/LBL)患者的2 期研究的更新数据。
在评估疗效的11例患者中,10例患者肿瘤缩小或消失,客观缓解率(ORR)为91%,其中8例患者完全缓解(CR),2例患者完全缓解伴血液学恢复不完全(CRi)。
一名T细胞淋巴母细胞淋巴瘤(T-LBL)患者4线治疗后复发,WU-CART-007治疗后,肿瘤病灶大幅度缩小甚至消失。

多年来,免疫疗法承载着人类对抗癌症的希望。随着免疫检查点抑制剂、细胞免疫疗法、肿瘤疫苗等逐渐取得进展,越来越多的癌症患者从中获益,甚至实现长期生存。
CAR-T细胞疗法是一款“热门”抗癌疗法,通过将T细胞取出体外,给T细胞安装上能够精准识别癌细胞的“导航”,并增殖、活化T细胞,让T细胞变得更强,并将增强后的T细胞回输至患者体内,以此来帮助T细胞战胜癌细胞。
印度CAR-T细胞产品talicabtagene autoleucel在B 细胞恶性肿瘤患者中具有显著效果
近日,《柳叶刀》发表了抗CD19嵌合抗原受体(CAR)T 细胞疗法 talicabtagene autoleucel 用于复发或难治性 B 细胞恶性肿瘤患者的 1/2 期研究结果。

共入组64名患者,有57名患者接受了talicabtagene autoleucel治疗,其中51名患者(36 名 B 细胞淋巴瘤患者和 15 名 B 细胞急性淋巴细胞白血病患者)可评估疗效。结果显示:总缓解率(ORR)为73%,也就是说37名患者肿瘤缩小或消失。
Talicabtagene autoleucel 是一种新型的人源化抗 CD19 CAR T 细胞疗法。早在2023 年便在印度获批用于治疗复发/难治性 B 细胞淋巴瘤和复发/难治性 B 细胞急性淋巴细胞白血病。该试验数据再次证明,Talicabtagene autoleucel在复发或难治性 B 细胞恶性肿瘤患者中具有较好的疗效。
cema-cel延长大 B 细胞淋巴瘤患者无进展生存期
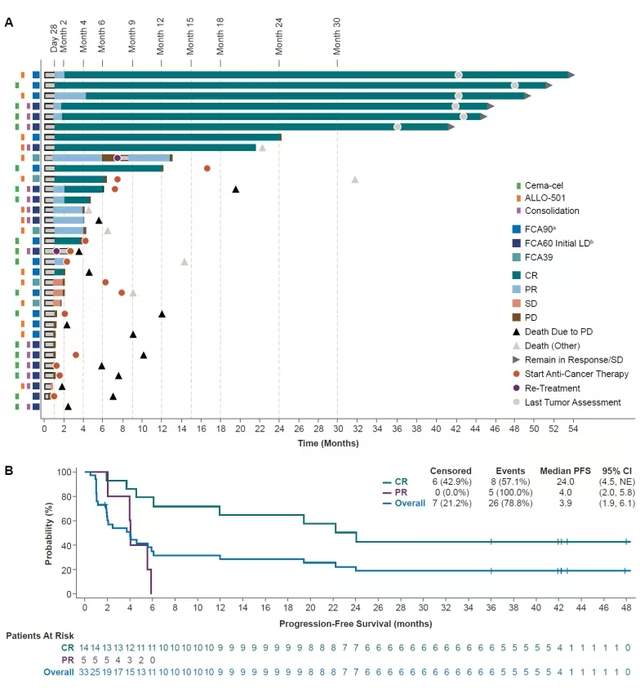
Cemacabtagene Ansegedleucel(cema-cel)是一款靶向CD19的同种异体CAR-T疗法,2月13日,全球顶尖肿瘤学期刊《Journal of Clinical Oncology》发表了Cemacabtagene Ansegedleucel/ALLO-501 治疗复发/难治性大 B 细胞淋巴瘤的I期ALPHA2/ALPHA 临床研究结果。
该试验共33名CAR-T细胞初治的大B细胞淋巴瘤患者接受治疗,结果显示:14例患者达到完全缓解(CR)状态,5名患者达到部分缓解(PR)状态,4例患者病情稳定(SD),中位缓解持续时间(DOR)为11.1个月,达到完全缓解状态的患者中位缓解持续时间为23.1个月,达到完全缓解状态的患者中位无进展生存期(PFS)为24个月,所有患者中位总生存期(OS)为14.4个月。
自首款CAR-T细胞疗法获批上市后,实体肿瘤患者便时刻期待自己有朝一日也可以用CAR-T细胞疗法来挽救自身。为了满足实体肿瘤患者的需求,科研人员夜以继日的探索。终于,CAR-T细胞疗法在实体肿瘤领域也取得了突破。
舒瑞基奥仑赛注射液纳入突破性治疗
近日,科济药业的CT041自体CAR T细胞注射液拟纳入突破性治疗,用于既往接受过至少二线治疗失败的Claudin18.2(CLDN18.2)表达阳性的晚期胃/食管胃结合部(G/GEJ)腺癌。

CT041(舒瑞基奥仑赛注射液)是一款针对Claudin18.2阳性的晚期消化系统肿瘤的CAR-T细胞候选产品。发表于《自然医学》的I期临床试验CT041-CG4006(NCT03874897)数据显示:疾病控制率高达96.1%(49),总缓解率为54.9%(28),其中27例患者实现部分缓解(PR),1例患者完全缓解(CR),中位缓解持续时间(mDOR)为6.4个月。

KT032有效治疗卵巢癌患者
KT032是一款靶向间皮素(MSLN)的CAR-T细胞疗法,2024年11月15日,《Genome Medicine》发表了KT032在MSLN阳性实体瘤(包括卵巢癌和间皮瘤)中的人体研究试验结果。

该试验共纳入8例MSLN阳性晚期复发性难治性卵巢癌患者和1例间皮瘤患者,共6例患者可评估了解,其中2例达到部分缓解(PR),4 例达到疾病稳定(SD)状态,疾病控制率(DCR)高达100%,中位总生存期(OS)为 10.5 个月。
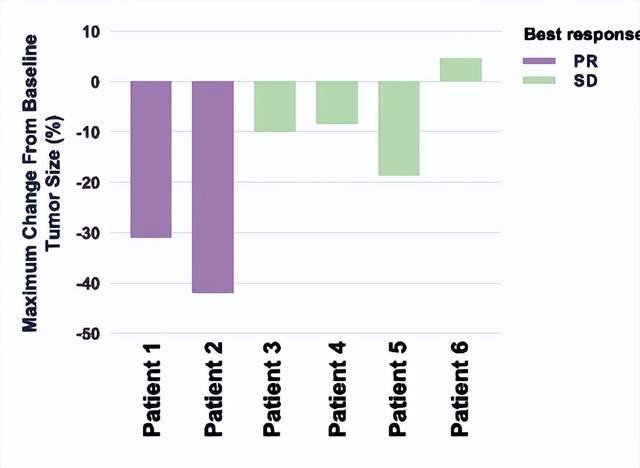
试验中患者肝转移病灶减少了31%,腹膜积液消失,癌抗原125(CA125)水平在CAR-T治疗32天后从1687 U/mL显著下降至150 U/mL。患者 2 的可测量病灶的总最大直径减少了42%,其他患者的肿瘤病灶或转移的变化不显著。

结语
近年来,免疫治疗在癌症治疗中取得重要进展,免疫检查点抑制剂、CAR-T、TCR-T等治疗方式层出不穷,为越来越多的癌症患者带来了治疗希望。截至目前,CAR-T细胞疗法已经在胃癌、肝癌、肾癌、胃癌、前列腺癌、结直肠癌、胰腺癌等多实体瘤临床试验中取得了显著疗效,并在多发性骨髓瘤、淋巴瘤、白血病等领域上市了多款产品。尽管面临许多挑战,但通过研究人员不断的探索和创新,有望克服障碍,推动CAR-T细胞疗法在实体瘤中蓬勃发展。