在利用气体的状态方程解题时,每个方程的研究对象都是一定质量的理想气体,但是在有些问题中,气体的质量可能是变化的。下面来谈谈求解这类问题的方法。
一、恰当选取研究对象,将“变质量问题”转化为“定质量问题”
运用理想气体状态方程解决问题时,首先要选取一定质量的理想气体作为研究对象。对于状态发生变化过程中,气体质量发生变化的问题,如充气,漏气等,如何选择适当的研究对象,将成为解题的关键。

例1、如图1(a)所示,一容器有孔与外界相通,当温度由300K升高到400K对,容器中溢出的气体质量占原来的百分之几?
解法一:选取气体温度为300K时容器中的气体作为研究对象,当温度升高后,有一部分气体溢出,我们假设溢出的部分被一个“没有弹性可以自由扩张的气囊”装着,如图1(b)。

这样,当气体温度升高后,容器中的气体与“囊”中的气体质量之和便与初始状态相等。于是,将“变质量问题”转化成了“定质量问题”。由于本题压强未发生变化,状态参量列出如下:







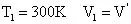

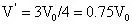
二、利用理想气体状态方程的推论,求解“变质量问题”

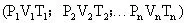

在利用此推论求解“变质量问题”时,要注意初状态的气体质量与末状态的各部分气体质量之和相等。


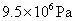

分析:根据题意可知,一定质量的气体由初状态变化到末状态时,分成了2个状态不同的部分,即

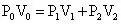

三、利用虚拟气体状态的方法求解“变质量问题”

分析:假设容器中原来的气体从状态1全部变为压强为1大气压,温度为300K的状态2,即




根据理想气体状态方程,则:




四、利用克拉珀龙方程(PV=nRT)求解“变质量问题”
例4、容积分别为9L,6L的A、B两容器,分别装有一定质量的同种理想气体,两容器用带阀门的细管相连,并分别置于300K和400K的恒温环境中,开始A、B中气压分别为10大气压和4大气压,打开阀门得重新平衡后,气体压强为多大?A中气体进入B中的部分占A中原有气体质量的百分之几?
分析:分别以A、B两部分气体作为研究对象,列出初末状态的参量如下:


根据克拉珀龙方程,则:

又因为初状态A、B两部分气体摩尔数之和等于末状态A、B两部分气体摩尔数之和,则有:

这样便很容易求出打开阀门重新平衡后气体的压强P=8大气压,A中气体进入B中的部分与A中原有气体质量之比为:
