诺瓦瓦克斯(Novavax)的新型蛋白基新冠疫苗获得美国食品药品监督管理局(FDA)批准。
这款名为Nuvaxovid的疫苗适用于老年人,以及12至64岁之间患有基础疾病、面临更高感染风险的人群。
Nuvaxovid由诺瓦瓦克斯与赛诺菲(Sanofi)合作开发,后者将根据里程碑协议向诺瓦瓦克斯支付1.75亿美元,未来还可能从疫苗销售中支付更多特许权使用费。

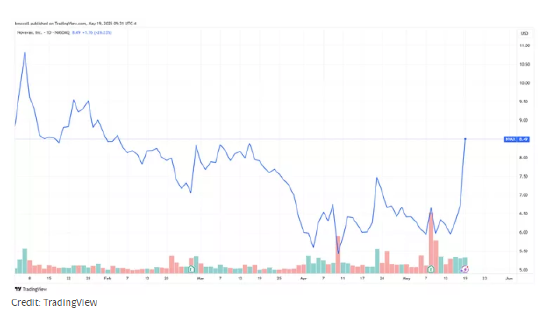
美国食品药品监督管理局(FDA)批准诺瓦瓦克斯新型新冠疫苗后,诺瓦瓦克斯(NVAX)股价周一开盘即飙升25%。
该制药商表示,FDA批准了其针对Nuvaxovid的生物制品许可申请(BLA)。这款疫苗适用于65岁及以上人群,以及12至64岁之间至少患有一种基础疾病、面临高感染风险的人群。Nuvaxovid与市场现有新冠疫苗的不同之处在于,它是蛋白基疫苗,而非mRNA疫苗。
这款疫苗由诺瓦瓦克斯与法国生物科技公司赛诺菲(SNY)合作开发。根据协议,赛诺菲将在BLA批准后向诺瓦瓦克斯支付1.75亿美元的里程碑款项。诺瓦瓦克斯指出,该合作对公司具有“多层价值”:赛诺菲将从今年起主导Nuvaxovid的商业化,诺瓦瓦克斯则有权“在未来所有疫苗接种季中,从独立新冠疫苗销售中获得持续的分层特许权使用费”。公司预计将于今年秋季商业化交付2025-2026版本的Nuvaxovid。
首席执行官约翰・雅各布斯(JohnJacobs)解释称,市场需求应会强劲,因为市场研究和联邦健康数据显示,“老年人和有基础疾病的人群最有可能季节性寻求新冠疫苗接种”。
截至周一,诺瓦瓦克斯股价年初至今累计下跌16%。