近期,美国德克萨斯大学奥斯汀分校助理教授王辉亮团队基于氢键有机框架(HOF,hydrogen-bondedorganicframework),开发了一种新型的超声可编程药物递送平台。
这项研究首次实现了通过非侵入性方式对深部脑区进行精准药物控释和神经调控:研究人员利用聚焦超声技术,在靶向脑区精确控制HOF载体中药物的激活释放,从而实现对特定神经元活动的时空精准操控。
根据在小鼠大脑的实验结果,该技术将传统化学遗传学的时间分辨率从几十分钟提升至3.6秒,并证明了其在9毫米深度仍可保持药物精准释放的能力。
该研究不仅为未来超声在精确分子操控奠定了理论基础,还为实现无创、精准和个性化医疗提供了新的技术手段,例如开发超声编程纳米机器人/药物,定向麻醉、定向免疫激活等。

日前,相关论文以《氢键有机框架作为超声可编程的递送平台》(H-bondedorganicframeworksasultrasound-programmabledeliveryplatform)为题发表在Nature[1]。
德克萨斯大学奥斯汀分校博士后研究员王文靓,以及合作者史彦庶博士、柴文瑞博士和KaiWingKevinTang博士为共同第一作者,王辉亮和陈邦林教授担任共同通讯作者。

“通过结合基因工程和药物工程开发的化学遗传学技术,将受体分子首先表达在目标神经元中,就可以通过特定的设计药物对特定的神经元进行选择性激活控制。”王辉亮表示。
与传统光遗传学使用的外源性光敏蛋白(通常源自细菌或海藻)相比,化学遗传学采用的受体分子与人体内源蛋白具有更高相似性,因而显著降低了免疫排斥风险。
这种受体分子与人自身的蛋白更为相似,因此免疫反应较低;而光遗传学中使用的光敏蛋白通常来源于细菌或海藻,可能会引发免疫反应。
尽管传统静脉注射给药方式在神经调控中已有应用,但其存在两个关键性技术瓶颈:首先是时间分辨率受限,药物从注射到靶向部位代谢激活通常需要30-60分钟,这严重制约了其在需要毫秒级响应的神经环路研究中的应用;其次是系统脱靶效应难以避免,药物在全身循环中可能引发非特异性作用。
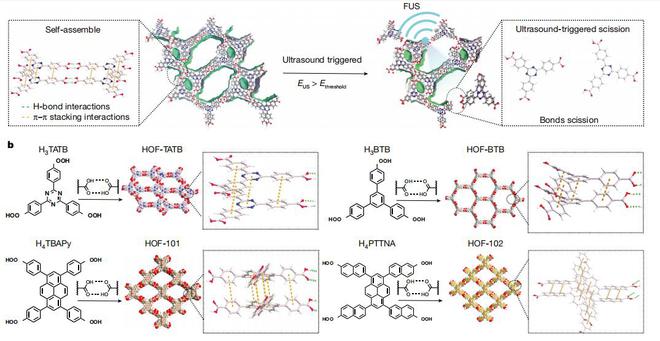
为解决这些实际需求,该课题组提出了通过超声波直接控制分子激活的技术,初步命名为超声编程的分子控制技术,也称为“超声分子手术刀”(ultrasonicmolecularscalple)。
研究人员设计了利用纳米粒子和超声波来激发的HOF递送体系。HOF是由小分子通过非共价键堆叠形成晶态多孔材料。通过聚焦超声产生的机械力场选择性地断裂分子键,实现了对药物释放的精准时空控制。
该体系分子的优势在于:结构确定、拓扑结构均一,生物可降解性优异;重复门槛低、易于批量生产;以及独特的超声点对点控制性能。
王文靓表示:“超声产生的机械场可以有效破坏HOF组装单元之间的非共价相互作用,实现选择性的框架激活,从而将装载的药物从分子框架中释放出来。我们的实验证明,可在3.6秒内实现有效的神经激活控制,与现有技术相比将响应延迟提高了数百倍。”
这种超声响应特性源于精心设计的分子工程策略:通过调控不同分子间的相互作用力,构建具有三维网络结构的智能载体,使其对超声刺激表现出可编程的响应阈值。
为深入解析作用机制,研究人员结合密度泛函理论计算,构建了“超声参数–分子结构–激活效率”三变量定量关系模型,深入揭示超声激活过程中分子响应的结构依赖性与能量敏感性。
在特定超声能量阈值下,分子激活百分比表现出明显的平台效应,呈现非线性响应特征。该规律符合吉布斯自由能变理论,揭示了超声能量调控分子构象转变的热力学本质,为实现药物激活的精准剂量控制提供了理论支持。
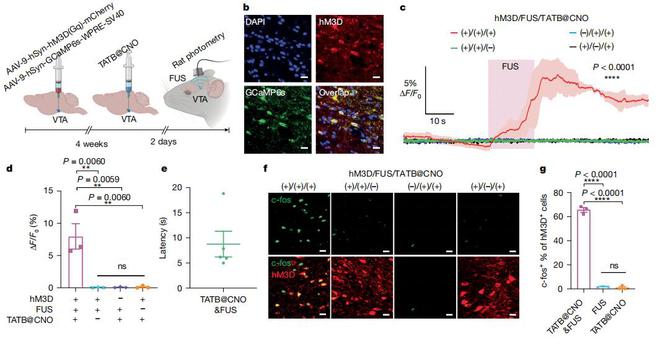
传统的药物,无论是口服还是通过静脉注射都会在全身释放。而该技术开发的超声可编程药物递送技术则实现了革命性突破——可以通过非侵入的方式精准确控制药物在特定位置、特定时间进行释放,因而在临床方面表现出应用潜力。
首先,可应用于需要高度选择性和时空依赖性的疾病治疗,例如癌症治疗和免疫治疗。
以癌症治疗为例,普通的小分子化疗药物在肿瘤部位的利用率很低,并且大部分药物会通过脏器代谢,同时对正常细胞造成严重损伤。与之对比的是,该技术将化疗药物装载到HOF体系中,通过静脉注射后避免药物在正常组织中的释放,从而减少对正常组织的损伤。
通过聚焦超声,可以精确地控制药物在病灶部位的激活,只在病灶部位杀死癌细胞,在降低药物脱靶性的同时提高利用率。同时,这种非侵入方式可以靶向控制药物在靶向部位的激活,降低副作用并提高疗效。
免疫治疗面临的一个主要问题是免疫反应过激,难以控制。该技通过定量、定点的免疫激活,为只激活特定部位的免疫反应提供保障,比如CAR-T细胞的激活,用于治疗免疫相关疾病或与基因的定向选择性表达相结合。
王文靓解释说道:“通过超声和定点药物激活,我们可以和CRISPR等技术联合应用,实现远程的精准分子操控用于疾病治疗。”
其次,该技术还对容易脱靶的分子治疗具有应用价值。目前,研究人员也在探索该技术应用在神经退行性疾病、心血管疾病、慢性疼痛和癫痫等疾病的应用。
在接下来的研究阶段,该课题组计划在分子反应动力学进行深入解释,并结合美国食品药品监督管理局(FDA,FoodandDrugAdministration)的要求,推动这项技术走向临床。
此外,研究人员还计划利用AI技术来辅助药物的设计和筛选。通过构建超声响应分子数据库和开发预测模型,以更高效地找到适合超声波激活的药物分子,从而推动该技术在更多疾病治疗中应用。
参考资料:
1.Wang,W.,Shi,Y.,Chai,W.etal.H-bondedorganicframeworksasultrasound-programmabledeliveryplatform.Nature638,401–410(2025).https://doi.org/10.1038/s41586-024-08401-0
运营/排版:何晨龙