
编者按
转移性前列腺癌在激素敏感阶段的治疗对患者的远期结局至关重要,因此,安全、有效的转移性激素敏感性前列腺癌(mHSPC)管理方案是前列腺癌领域研究的重点。如今,以雄激素剥夺治疗(ADT)为基础的联合治疗方案已成为mHSPC的一线标准治疗方案。然而,临床中新开始ADT治疗的患者发生激素治疗相关常见副作用时应如何管理?mHSPC阶段即接受三联强化方案治疗的患者进展后的治疗方案及其结局如何?治疗后早期的生化指标与远期结局预后是否相关?本期“益腺学院”聚焦2024年ASCO年会,特邀中山大学附属第三医院罗云教授,深入解读mHSPC相关研究进展,探索当前临床实践中mHSPC管理方案的优化方向,并分享其专业见解。
专家简介
罗云 教授
中山大学附属第三医院
主任医师,博士生导师
中山大学附属第三医院 泌尿外科
中山大学附属第三医院泌尿外科副主任
中山大学附属第三医院岭南医院泌尿外科主任
中山大学-McGill大学联合培养博士
广东省杰出青年医学人才
中华医学会泌尿外科分会工程学组委员
中国医师协会泌尿外科分会青委会委员
广东省医学会泌尿外科分会青委会副主任委员
广东省医师协会泌尿外科分会常务委员
Abstract LBA5004 MANCAN2:自助式认知行为疗法(CBT)在接受ADT治疗的前列腺癌患者中管理潮热和盗汗(HFNS)症状的多中心、随机对照研究[1]
研究背景
接受ADT治疗的患者80%会发生HFNS,可能降低患者的生活质量(QOL)且影响ADT的依从性。然而缓解HFNS的方法有限。既往研究发现,在仅有很少指导的情况下,自助式CBT可在6周时减少ADT治疗引起的HFNS。本研究探索了在前列腺癌护理专家(CNS)团队指导下自助式CBT的长期影响。
研究方法
MANCAN2是一项在英国前列腺癌科室进行的多中心、随机对照研究和流程评估。纳入标准:局限性或晚期前列腺癌;未来计划接受ADT≥ 6个月;HFNS问题量表评分≥ 2。患者按每个小组6-8人,以1:1随机分配至常规治疗组或CBT+常规治疗组,并根据中心、队列和治疗意向分层。CBT是一项为期4周的自助式干预措施(手册、放松音频、呼吸和放松练习等),在干预前和干预后以小组形式由前列腺癌CNS团队指导进行。主要目的为评估在常规治疗的基础上增加CBT较基线能否降低6个月时的HFNS问题量表评分(混合线性回归)。次要终点为6个月时的HFNS问题量表评分、HFNS频次、HFNS信念行为量表评分、QOL(EORTC QLQ-C30量表评分、症状[焦虑、抑郁、情绪、睡眠量表],混合logistic回归)、ADT依从性(卡方检验)。
研究结果
共162例患者进行了随机化分组(每组81例),其中117例返回了6个月时HFNS问题量表评分。两组间基线特征平衡。平均CBT依从性为85%。尽管在第6周时观察到常规治疗 vs. CBT+常规治疗两组间的HFNS问题量表评分有差异(平均值:4.47 vs 3.79,95% CI -1.26~-0.09,P=0.025),但6个月时两组间的平均HFNS问题量表评分无显著差异(平均值:4.08 vs. 4.04,95% CI -0.89~0.80;P=0.967;详见图 1)。

图 1. 两组基线、6周和6个月时的HFNS问题量表评分
在6周时,CBT组患者每周HFNS频次较高(中位值:54.2 vs. 59.4,95% CI 0.22~10.19;P=0.04),抑郁评分较低(中位值:7.19 vs. 6.19,95% CI -1.88~-0.12;P=0.03),焦虑评分较低(中位值:4.25 vs. 3.39,95% CI -1.64~-0.08;P=0.03)。CBT组患者6个月时关于开放性和幽默的积极信念评分更高(中位值:4.92 vs. 4.59,95% CI -0.63~-0.03;P=0.03),HFNS信念行为量表评分的其他指标、QOL、情绪和睡眠质量等在两组间没有显著差异。此外,6个月时CBT组患者对ADT的依从率显著高于常规治疗组(100% vs. 86.2%,P=0.006)。
研究结论
在常规治疗的基础上增加CBT可改善接受ADT的前列腺癌患者HFNS的短期严重程度,但未能维持6个月,未来应探索CBT的长期影响。
罗云教授点评
作为激素依赖性的肿瘤,前列腺癌各阶段的治疗中都可能有ADT的参与,而对于局部晚期或转移性前列腺癌,ADT更是主要治疗手段和各种联合治疗的基础[2],且常需长期应用。作为临床医生,我们往往更关注ADT的心血管风险、骨健康风险等可能带来严重不良后果的副作用,而对于潮热盗汗这类内分泌治疗最常见的不良事件,则关注不足。因为通常觉得这类不良反应并不严重,患者习惯了或者克服一下就好,不会造成严重后果。但其实,潮热盗汗会给患者,特别是刚开始接受内分泌治疗的患者带来严重的生活和心理困扰,加重负面情绪,影响患者生活质量,甚至影响用药的依从性,从而影响治疗结局。既往研究表明,一些激素类、抗抑郁或抗癫痫药对ADT引起的潮热有一定作用[3],本次大会摘要LBA12004亦报道了奥昔布宁可以有效降低前列腺癌内分泌治疗相关的潮热频率[4],但目前这些药物治疗的证据仍不充分,更重要的是,这些药物本身也会带来一定的副作用,因此一般仅考虑在症状比较严重的患者中应用。
而非药物的干预措施,例如针灸、瑜伽等也一直在探索,其中,心理学中的CBT简单、安全且容易坚持,近年来,CBT在缓解女性乳腺癌患者的内分泌治疗相关潮热中已有报道取得了较好的效果[5],但在前列腺癌患者中的研究应用则相对较少,既往MANCAN单中心研究显示,与常规治疗相比,CBT可在第6周时显著降低患者HFNS问题评分和HFNS频次,并在第32周时持续改善[6]。本次大会LBA5004报道的MANCAN2研究则进一步在更多的中心和患者中进行了探索,结果显示,第6周时CBT组的HFNS问题评分、焦虑、抑郁评分均显著较低,虽然该改善未能持续至6个月。但更重要的是,6个月时常规治疗组有13.8%的患者中止了ADT,而CBT组则全部继续治疗,这说明CBT在缓解前列腺癌HFNS症状和提高药物治疗的依从性方面均有临床应用前景。我们中国临床工作者除了对治疗疾病本身不断精进外,也应学习和实践先进的患者管理和教育理念,采用多种手段全面提高患者的疾病认知、常见副作用的管理和用药依从性,特别是在如前列腺癌这种需要长期管理的疾病中,关注并尊重患者的需求和感受,全面提高患者的生活质量。
Abstract 5083 mHSPC患者接受达罗他胺或安慰剂治疗进展后的生存情况:ARASENS研究事后分析[7]研究背景
达罗他胺是一种结构独特且高效的雄激素受体通路抑制剂(ARPI)。在ARASENS(NCT02799602)研究中,尽管大多数(75.6%)安慰剂+ADT+多西他赛组患者接受了后续治疗,但达罗他胺+ADT+多西他赛组患者的死亡风险降低了32.5%。与安慰剂相比,达罗他胺还可延缓患者进展至转移性去势抵抗性前列腺癌(mCRPC)的时间(中位值:未达到 vs. 19.1个月)。本次事后分析报道了ARASENS研究中患者进展后的后续抗肿瘤治疗和相关生存情况。
研究方法
mHSPC患者按1:1随机接受达罗他胺(600mg,每日两次)+ADT+多西他赛或安慰剂+ADT+多西他赛治疗。在治疗停止后,患者进入长期生存随访阶段,以评估患者后续抗肿瘤治疗方案和生存结局。采用Kaplan-Meier法估计进展后生存期,定义为患者首次接受后续抗肿瘤治疗至死亡的时间。
研究结果
在1305例(达罗他胺组n=651;安慰剂组n=654)接受治疗的患者中,达罗他胺组的315例患者和安慰剂组的409例患者进入随访期,分别有57%(n=179)和76%(n=374)的患者接受了后续抗肿瘤治疗,阿比特龙和恩扎卢胺是后续首个抗肿瘤治疗中最常用的方案(详见表1)。
表1. ARASENS研究中患者后续首个抗肿瘤治疗方案
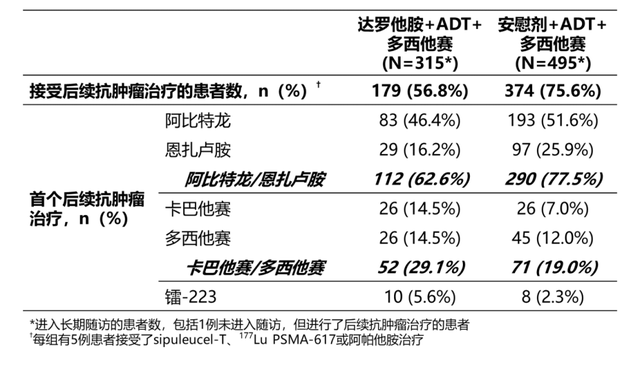
在达罗他胺组中,90%的患者使用ARPI或化疗作为首个后续治疗方案。不同后续治疗方案间患者进展后的生存率差异较小(详见图2),表明达罗他胺进展后换用另一种ARPI相较非ARPI方案(主要是化疗)无法带来更多生存获益。
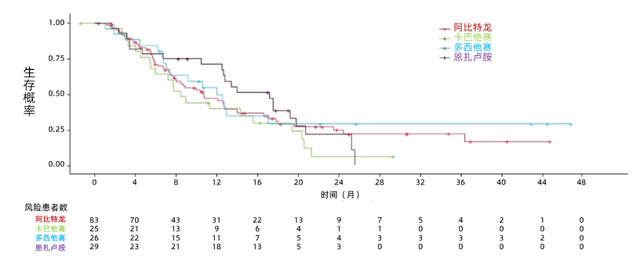
图 2. 达罗他胺+ADT+多西他赛组不同后续首个抗肿瘤方案的OS
而在安慰剂组中,大多数(78%)患者后续首个抗肿瘤方案为ARPI,与非ARPI方案相比,可观察到更多生存获益(中位值:23.0个月 vs. 13.5个月),详见图3。
 图 3. 安慰剂+ADT+多西他赛组进展后不同后续首个抗肿瘤方案的OS
图 3. 安慰剂+ADT+多西他赛组进展后不同后续首个抗肿瘤方案的OS
研究结论
与安慰剂+ADT+多西他赛相比,达罗他胺+ADT+多西他赛方案延长了患者的总生存期(OS),并延迟患者进展至mCRPC时间。达罗他胺组患者在进展后所有后续治疗方案之间生存率相似。接受安慰剂+ADT+多西他赛治疗的患者较快进展至mCRPC,既往未接受过ARPI治疗的患者进展后使用ARPI方案可延长生存期。
罗云教授点评
近年来,新型内分泌治疗药物在前列腺癌各阶段的众多重磅临床试验不断改写着前列腺癌的治疗格局。其中,ARASENS研究显示,在ADT+多西他赛的基础上联用达罗他胺可显著延长mHSPC患者的OS(未达到 vs. 48.9个月,HR=0.68,P<0.0001)[8]。基于此结果,CSCO指南对达罗他胺三联方案用于mHSPC高瘤负荷和低瘤负荷人群给予了1A类I级推荐[9]。在2023年CSCO发布的《中国晚期前列腺癌诊疗现状蓝皮书》中,对23个省级行政单位共228位临床医生的调研结果显示,虽然可能基于不良反应管理和药物可及性的考量,实际中选择三药联合方案的医生比例偏低,但临床医生仍然认可ARPI+ADT+化疗三联方案[10]。
随着强化治疗前移逐渐被认可,随之而来的另一个问题也摆在了我们面前——几乎所有mHSPC患者在一定时间的内分泌治疗后最终都会进展为mCRPC [2],而mCRPC阶段的治疗选择有限,在mHSPC阶段就已经应用了ARPI+ADT+化疗三联方案的患者似乎面临无药可用的情况,那是否应将这些强化治疗的手段留待进展至mCRPC后再应用呢?本次大会摘要5083则为我们提供了证据和思考。该研究为我们解答了3个问题:第一,在mHSPC阶段应用ARPI+ADT+化疗三联方案可显著延缓进展至mCRPC的时间;第二,mHSPC阶段应用三联方案的患者进展后换用另一种ARPI或接受化疗仍可继续获益;第三,在mHSPC阶段应用三联方案的患者总体OS也显著更长。综上所述,对于能够耐受的患者,在更早期的mHSPC阶段即使用ARPI+ADT+化疗三联疗法不仅能延长患者OS,更能延长患者处于mHSPC疾病阶段的时间,而该阶段患者的总体生活质量优于mCRPC阶段(见图4)。该研究的结果也进一步支持了晚期前列腺癌“联合治疗增效,组合优于序贯”的治疗理念。

图 4. ARASENS研究中两组患者疾病进展与生存情况
Abstract 5079 接受恩扎卢胺治疗的mHSPC患者7个月时前列腺特异性抗原(PSA)水平对预后的影响:ENZAMET(ANZUP 1304)研究的Landmark分析[11]
研究背景
ENZAMET(NCT02446405)研究显示,与标准非甾体类抗雄药(NSAA)+睾酮抑制(TS)±多西他赛相比,恩扎卢胺+TS±多西他赛可延长mHSPC患者的OS。本次评估了ENZAMET研究中患者随机化后7个月时的PSA水平及其与OS的关系。
研究方法
纳入随机化后至少随访7个月,且有PSA数据和治疗结局的患者。在7个月时根据SWOG 9346和CHAARTED研究中已确定的预后分层指标(即开始治疗7个月时PSA≤0.2 ng/ml和>0.2 ng/ml)进行Landmark分析。
研究结果
在所有ENZAMET研究的患者中,7个月时646/1125例(57%)患者PSA达到了≤0.2 ng/ml,其中,NSAA组为271/562例(48%),恩扎卢胺组为375/563例(67%)。在NSAA组中,PSA≤0.2 ng/ml vs. PSA>0.2 ng/ml的患者5年OS率分别为71% vs. 36%;在恩扎卢胺组则为74% vs 43%。根据关键预后因素(高瘤负荷 vs. 低瘤负荷)和是否联用多西他赛分组,7个月时PSA≤0.2 ng/ml和PSA>0.2 ng/ml的患者比例及其5年OS率详见表2,对OS的Landmark分析详见图5和图6。
表2. 不同治疗组不同肿瘤负荷患者PSA应答与5年OS率
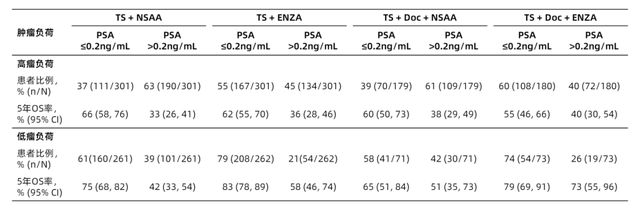
 图5. 高瘤负荷(HV)患者OS的Landmark分析
图5. 高瘤负荷(HV)患者OS的Landmark分析

图6. 低瘤负荷(LV)患者OS的Landmark分析
按照不同PSA水平分析患者前列腺癌与非前列腺癌特异性死亡率,在645例PSA≤0.2 ng/ml的患者中,5年内共151例患者死亡,其中39例(26%)为非前列腺癌特异性死亡;在459例PSA>0.2 ng/ml的患者中,5年内共257例患者死亡,其中36例(14%)为非前列腺癌特异性死亡,两组的前列腺癌特异性死亡率有显著差异(详见表3和图7)。
表3. 不同PSA水平患者的5年前列腺癌特异性死亡率
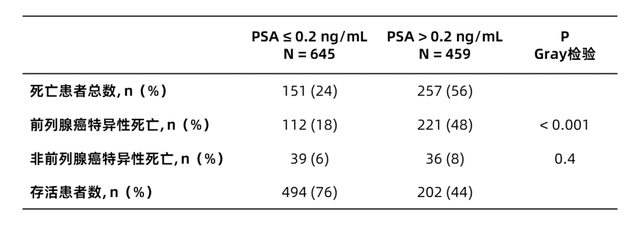
 图7. 不同PSA水平患者的肿瘤特异性死亡分析
图7. 不同PSA水平患者的肿瘤特异性死亡分析
研究结论
无论治疗方案和预后因素(高瘤负荷 vs. 低瘤负荷)如何,7个月时PSA最低值≤0.2 ng/ml均与较长的OS相关。联合恩扎卢胺提高了各治疗组达到PSA≤0.2 ng/ml的患者比例。7个月时达到PSA最低值≤0.2 ng/ml的患者前列腺癌特异性死亡率更低。
罗云教授点评
PSA是前列腺癌诊疗中最重要的生物标志物,贯穿前列腺癌管理的始终。根据一项对中国前列腺癌研究协作组专家的调研,92%的专家首选PSA动力学指标,如PSA50、PSA90或PSA≤0.2 ng/ml作为治疗应答初步判定的指标[12]。本次大会摘要5079显示,在ENZAMET研究中,不论治疗方案或肿瘤负荷,7个月时PSA深度缓解均与长期OS获益相关。这与既往其他大型研究的结果一致,例如CHAARTED研究事后分析显示,在接受ADT±多西他赛的mHSPC患者中,7个月时PSA降至≤0.2 ng/ml与更长的OS相关[13]。ARASENSE研究事后分析结果显示,无论患者肿瘤负荷高低,在治疗6个月时达到PSA<0.2 ng/ml的患者进展至CRPC时间、至PSA进展时间和OS结果都更优[14]。这一方面可为今后新药的临床开发带来一定参考和启发,另一方面则提示临床医生,mHSPC患者治疗后PSA的快速、深度降低可预示远期获益,这对于患者预期管理以及后续治疗方案的制定都有着非常重要的意义。当然,我们也要充分认识到,PSA虽然非常重要,但只是疗效监测和疾病管理中的指标之一。对于晚期前列腺癌,我们同样要关注睾酮水平、影像学检查等其他随访结果,方能对疾病状态有全面的掌握,及时评估和调整治疗方案。
小结
总体而言,mHSPC的优化管理需要多方面的努力和探索,在探索新的治疗方案使患者生存期得到延长的同时,也应关注药物副作用的管理,从而提高患者的依从性和生活质量。此外,对各种药物最优治疗顺序的研究以及更有效的能预测远期疗效的生物标志物的探索也将更好地助力患者的长程管理,全面改善患者的生存和生活质量。
参考文献:
[1] CRABB S J, MORGAN A, STEFANOPOULOU E, et al. MANCAN2: A multicentre randomised controlled trial of self-help cognitive behavioural therapy (CBT) to manage hot flush and night sweats (HFNS) symptoms in patients with prostate cancer receiving androgen deprivation therapy (ADT).[J/OL]. Journal of Clinical Oncology, 2024, 42(16_suppl): LBA5004-LBA5004.
[2] 魏强. 前列腺癌诊断治疗指南[M]//黄健, 张旭. 中国泌尿外科和男科疾病诊断治疗指南:2022 版. 1 版. 北京: 科学出版社, 2022: 130-216.
[3] 中国医促会泌尿健康促进分会, 中国研究型医院学会泌尿外科学专业委员会. 前列腺癌经典内分泌治疗安全共识[J/OL]. 现代泌尿外科杂志, 2018, 23(4): 248-258.
[4] STISH B J, MAZZA G L, NAUSEEF J T, et al. Alliance A222001: A randomized, double-blind, placebo controlled phase II study of oxybutynin versus placebo for the treatment of hot flashes in men receiving androgen deprivation therapy. [J/OL]. Journal of Clinical Oncology, 2024, 42(16_suppl): LBA12004-LBA12004.
[5] MANN E, SMITH M J, HELLIER J, et al. Cognitive behavioural treatment for women who have menopausal symptoms after breast cancer treatment (MENOS 1): a randomised controlled trial[J/OL]. The Lancet. Oncology, 2012, 13(3): 309-318.
[6] STEFANOPOULOU E, YOUSAF O, GRUNFELD E A, et al. A randomised controlled trial of a brief cognitive behavioural intervention for men who have hot flushes following prostate cancer treatment (MANCAN)[J/OL]. Psycho-Oncology, 2015, 24(9): 1159-1166.
[7] Marc-Oliver Grimm, Matthew Raymond Smith, Maha H. A. Hussain, et al. Post-progression survival of patients with metastatic hormone-sensitive prostate cancer (mHSPC) who received darolutamide or placebo: Post hoc analysis of ARASENS. [J/OL]. Journal of Clinical Oncology, 2024, 42(16_suppl): 5083-5083.
[8] Smith MR, Hussain M, Saad F, et al. Darolutamide and Survival in Metastatic, Hormone-Sensitive Prostate Cancer. N Engl J Med. 2022 Mar 24;386(12):1132-1142.
[9] 中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)前列腺癌诊疗指南[M]. 北京: 人民卫生出版社, 2022.
[10] 中国临床肿瘤学会(CSCO). 中国晚期前列腺癌诊疗现状蓝皮书[M].
[11] Ronan Andrew Mc Laughlin, Hayley Thomas, Ian D. Davis, et al. Prognostic implications of PSA levels at 7 months in metastatic hormone-sensitive prostate cancer treated with enzalutamide: Landmark analysis of ENZAMET (ANZUP 1304).[J/OL]. Journal of Clinical Oncology, 2024, 42(16_suppl): 5079-5079.
[12] 中国前列腺癌研究协作组, 叶定伟, 黄健. CPCC晚期前列腺癌中国专家共识——转移性激素敏感性前列腺癌起始应用新型内分泌治疗的全程管理(2022年版)[J/OL]. 中国癌症杂志, 2022, 32(12): 1242-1259.
[13] HARSHMAN L C, CHEN Y H, LIU G, et al. Seven-Month Prostate-Specific Antigen Is Prognostic in Metastatic Hormone-Sensitive Prostate Cancer Treated With Androgen Deprivation With or Without Docetaxel[J/OL]. Journal of Clinical Oncology: Official Journal of the American Society of Clinical Oncology, 2018, 36(4): 376-382.
[14] SAAD F, HUSSAIN M H A, TOMBAL B, et al. Deep and Durable Prostate-specific Antigen Response to Darolutamide with Androgen Deprivation Therapy and Docetaxel, and Association with Clinical Outcomes for Patients with High- or Low-volume Metastatic Hormone-sensitive Prostate Cancer: Analyses of the Randomized Phase 3 ARASENS Study[J/OL]. European Urology, 2024.
声明
本视频/资讯/文章是由益普生医学团队编辑/医疗卫生专业人士撰写提供,旨在用于医疗卫生专业人士间的学术交流,不支持以任何形式转发给非医疗卫生专业人士;如有违反,责任自负;转发给其他医疗卫生专业人士时,也请自觉保护知识产权。
本视频/资讯/文章的内容不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。内容中出现任何药品并非为广告推广目的,医疗卫生专业人士如进行处方,请严格遵照该药品在中国批准使用的说明书。益普生不承担任何相关责任。
DIP-CN-012250 有效期至2025年6月18日
编辑:Nobady
审核:Rudolf
排版:Gardenia
执行:Gardenia
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
