
聚前沿文献之声,解泌尿学术之惑

聚前沿文献之声,解泌尿学术之惑,这里是聚焦前列腺癌的《菲长视野 · 前献解泌》专栏。
本期与我们用声音见面的是复旦大学附属中山医院徐磊教授,他将与大家一同分享一项近日发表于《JAMA internal medicine》杂志(影响因子:22.5)的有关前列腺癌患者主动监测(active surveillance,AS)使用情况及相关变量的研究。

AS已成为低风险和部分有利中风险前列腺癌患者的标准治疗,AS旨在监测癌症的进展,以便在癌症进展时提供根治性治疗。截至2015年的数据显示,美国的AS使用率正在上升,已达42%。本研究通过最新发布的国家数据,评估了截至2018年的AS使用情况以及与之相关的变量[1]。
研究方法本项横断面研究对2022年5月15日至9月1日期间的去标识化数据进行了分析。根据美国国家综合癌症网络(National Comprehensive Cancer Network,NCCN)的定义,使用监测、流行病学和最终结果(Surveillance,Epidemiology and End Results,SEER)-前列腺观察等待(watchful waiting,WW)数据库识别2010年至2018年期间,年龄>40岁的低风险和有利中风险前列腺癌患者。SEER-WW数据库包含一个额外变量,表明患者是选择了AS还是WW。与AS不同的是,WW不监测癌症进展,而是观察直至出现临床症状。治疗方法不明或临床信息缺失的男性被排除在外。
研究分别采用Cochran-Armitage检验(单侧)和线性回归分析评估治疗年龄的时间趋势和变化。多因素Logistic回归分析用于评估AS/WW与根治性前列腺切除术或放射治疗的相关性。敏感性分析仅纳入年龄≤70岁的男性患者,因为他们更有可能接受AS而不是WW,对信息未知或缺失的患者进行多重插补(multiple imputation,MI)分析。统计学意义定义为双侧P=0.05。
研究结果● 低风险和有利中风险患者前列腺癌管理的时间趋势

2010年至2018年,在低风险患者中,AS/WW使用率从16.4%增加到59.9%(图1A);在有利中风险患者中,AS/WW使用率从7.8%增加到21.8%(P<0.001)(图1B)。

图1 2010-2018年美国低风险和有利中风险前列腺癌管理的时间趋势
接受AS/WW的低风险前列腺癌患者的中位年龄从65(四分位距[interquartile range,IQR],60-71)岁降至64(IQR,59-69)岁;平均年变化为-0.15(标准误[standard error,SE],0.02)岁,P<0.001;有利中风险前列腺癌患者的中位年龄从70(IQR,64-76)岁降至67(IQR,61-71)岁;平均年变化为-0.20(SE,0.04)岁,P<0.001。
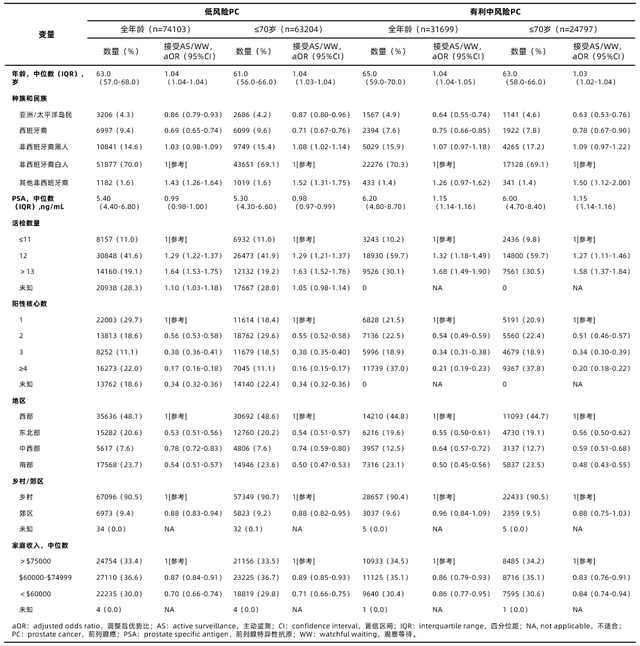
多因素分析显示,较高的收入与选择AS/WW相关(表1)。活检核心阳性数量与选择根治性治疗的几率增加相关。在低风险前列腺癌患者中,活检核心阳性数量为2相比活检核心阳性数量为1的调整后优势比(adjusted odds ratio,aOR)(95%置信区间[confidence interval,CI])为0.56(0.53-0.58)。与白人男性相比,亚裔/太平洋岛民和西班牙裔男性选择AS/WW的几率更低,而乡村地区与低风险患者选择根治性治疗相关。对年龄≤70岁前列腺癌患者的敏感性分析和插补数据集显示了类似的结果(表1)。
表1 低风险或有利中风险前列腺癌患者选择AS/WW与根治性治疗几率的多因素Logistic回归分析
本研究结果显示,截至2018年,美国前列腺癌患者的AS使用率持续上升,低风险前列腺癌的AS使用率增加到59.9%,有利中风险前列腺癌的AS使用率增加到21.8%。但在多次活检呈阳性的人群以及少数民族、低收入群体或生活在农村地区的人群中,AS的使用率较低。
专家有话说前列腺癌是全球男性最常见的恶性肿瘤之一,严重威胁男性的生命健康。近年来,随着医学技术的不断进展和对前列腺癌认知的不断深入,前列腺癌的治疗手段日益丰富,患者生存得到了显著改善。目前,国内外在前列腺癌手术设备以及技术、治疗药物的可及性等方面相当接近,但在早期前列腺癌AS的选择与应用方面仍存在显著差异。
前列腺癌相对惰性的特点是AS应用的前提。AS旨在监测癌症的进展,在不影响总生存的前提下,推迟可能的根治性治疗并减少治疗可能引起的副作用,避免过度治疗并提高患者生活质量。本研究分析了2010年-2018年间,美国低风险和有利中风险前列腺癌患者AS/WW的使用情况及影响因素。结果表明,随着时间推进,AS/WW的使用率显著提升,且接受AS/WW的患者也更加年轻。此外,活检阳性针数、人种以及乡村等因素也与AS的使用率有关。可以说,不同的医疗环境和文化差异导致了国内外前列腺癌AS的使用差异,这一策略的推广与落实需要患者的积极参与、配合。此外,在前列腺癌AS过程中存在病理升级的风险,需要我们严格选择合适的患者人群。相信随着未来我国早期前列腺癌的患者比例不断提高,患者和医生对AS认知以及接受度的提高,我们可以通过建立规范的筛选与随访标准,在临床实践中深入探索,惠及更多早期前列腺癌患者。
AS是早期前列腺癌的治疗方案之一,而对于局部晚期/转移性前列腺癌,以雄激素剥夺治疗(androgen deprivation therapy,ADT)为基础的联合治疗已成为新的标准。曲普瑞林作为代表性的ADT药物之一,在前列腺癌治疗领域发挥着基石作用,其6月剂型已于2023年6月在我国获批,同时具备1月、3月、6月三种不同剂型,为临床医生和患者带来更加灵活的治疗选择。研究显示,曲普瑞林6月剂型可以持续降低患者睾酮水平,一项包含9项前瞻性研究的汇总分析[2],纳入920例晚期/转移/局部治疗后生化复发的前列腺癌患者,使用曲普瑞林治疗2-12个月。结果显示,曲普瑞林治疗第3、6、9和12个月时,睾酮水平<20 ng/dL的患者比例分别为92%、93%、90%和91%。研究结束时,接受曲普瑞林1月、3月和6月剂型治疗患者的血清睾酮中位数分别为2.9(2.9-6.5)、50(2.9-8.7)和8.7(5.8-14.1)ng/dL。曲普瑞林6月剂型治疗的第3、6、9和12个月时,睾酮水平<20 ng/dL的患者比例分别为97%、94%92%和91%。
此外,曲普瑞林6月剂型对初治和转药患者均可有效降低前列腺特异性抗原(prostate specific antigen,PSA)。一项真实世界、回顾性的、非干预研究[3],纳入了88例接受6月剂型曲普瑞林治疗的转移性前列腺癌患者,其中47例初始接受曲普瑞林6月剂型治疗,41例由促性腺激素释放激素激动剂(gonadotropin-releasing hormone agonist,GnRH-a)1月/3月剂型更换为曲普瑞林6月剂型治疗。结果显示,换用曲普瑞林6月剂型后,患者的检查次数减少46.8%、PSA检测次数减少46.8%、注射次数降低26.6%(P均<0.0001);患者与医疗保健系统的互动次数减少41.5%,降低了患者的医疗成本。此外,在治疗12个月时,初始6月剂型曲普瑞林治疗患者中位PSA从诊断时的23.50 ng/mL下降为1.30 ng/mL,更换为6月剂型曲普瑞林治疗患者中位PSA从换药时的0.35 ng/mL下降为0.24 ng/mL[3],揭示了曲普瑞林6月剂型无论对初治亦或是换药患者均可有效降低PSA,疗效稳定。
曲普瑞林长效剂型在强效持续降低患者睾酮和PSA的同时,进一步减少注射次数,提高了患者治疗的便利性与依从性,有望成为前列腺癌长程管理的得力臂助。
专家简介
徐磊 教授
复旦大学附属中山医院
复旦大学附属中山医院泌尿外科副主任医师,硕士生导师
英国伦敦大学玛丽女王学院Barts医学院博士
英国伦敦大学学院医院泌尿外科 Honorary Academic Urologist
上海市医学会泌尿分会前列腺组委员
中华医学会泌尿外科协会(CUA)青委肿瘤学组
欧洲泌尿外科协会会员,韩国泌尿外科协会会员
2020上海市医学会泌尿外科分会青年英才
入选哈佛全球临床研究学者项目,CUA/CUDA BTB人才培养工程(加拿大蒙特利尔大学中心医院)
参考文献
1. Al Hussein Al Awamlh B, et al. JAMA Intern Med. 2023;183(6):608-611.
2. Breul J, et al. Adv Ther. 2017 Feb;34(2)513-523.
3. Cornford P, et al. Oncol Ther. 2018, 6(2) 173-87.
编辑:Rudolf
审校:Nobody执行:Gardenia本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
DIP_PC-CN-000196
DIP_PC-CN-000195
扫码进入“菲长视野”专区
查看更多前列腺癌前沿资讯
