缺血性视网膜病变(ischemic retinopathy, IR),包括糖尿病性视网膜病变(diabetic retinopathy, DR)、早产儿视网膜病变(retinopathy of prematurity, ROP)和年龄相关性黄斑变性(age-related macular degeneration, AMD),是失明的主要原因。异常血管生成是缺血性视网膜病变的关键过程,但其潜在的病理机制尚未完全阐明。

近日,天津医科大学朱宪彝纪念医院陈莉明教授团队在国际知名期刊Nature Communications发表了题为“Endothelial AGGF1 promotes retinal angiogenesis by coordinating TNFSF12/FN14 signalling”的原创学术论文,揭示了内皮AGGF1(血管生成因子1)依赖性视网膜病理性新生血管形成的潜在机制,并提供了一种有效治疗缺血性视网膜病变的新思路。
前言

研究背景及方法
AGGF1是一种新型血管生成因子,在内皮细胞中高度表达,并表现出与VEGF相似的功能,可促进内皮细胞增殖、迁移和血管生成。然而,AGGF1在缺血性视网膜病变中的作用尚未阐明。该研究运用蛋白组学分析、免疫共沉淀及免疫荧光染色等方法评估了AGGF1在视网膜病理性新生血管形成中的作用和机制。
研究结果
01AGGF1在缺血性视网膜病变中上调
db/db小鼠(2型糖尿病模型)的视网膜组织蛋白组学分析发现AGGF1表达升高,在Western blot和免疫组织化学染色中得到进一步证实。PDR(增殖性糖尿病视网膜病变)患者视网膜和神经节细胞层厚度变薄,玻璃体液和房水中AGGF1表达明显升高。

图1. AGGF1在缺血性视网膜病变中的表达水平
a. 增殖性糖尿病视网膜病变(PDR)患者的代表性眼底荧光造影(FFA)和光学相干断层扫描(OCT)图像;b. 患者房水中AGGF1水平的ELISA分析结果。
02内皮细胞AGGF1缺失显著改善氧诱导视网膜病变(OIR)小鼠的视网膜病理性新生血管形成和血管闭塞
研究者发现AGGF1主要表达在血管内皮细胞,在OIR小鼠视网膜中表达显著上调。这些结果提示,AGGF1可能参与临床缺血性视网膜病变病理性新生血管形成。内皮细胞Aggf1缺失显著减轻视网膜病理性新生血管形成及血管闭塞。

图2.内皮细胞AGGF1缺失改善视网膜病理性血管新生
a. 在P17时常氧和OIR下全视网膜中AGGF1蛋白的表达和定位; b, c. Aggf1fl/fl 和 Cdh5-Cre Aggf1fl/fl 常氧和OIR小鼠P17时的全视网膜FITC染色代表图。
03AGGF1促进TNFSF12与Fn14的结合以增加血管生成
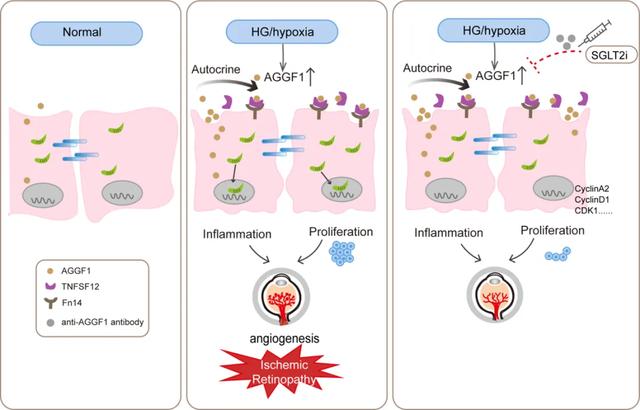
那么AGGF1调控视网膜病理性新生血管形成的机制是什么呢?AGGF1通过与肿瘤坏死因子配体超家族成员12(TNFSF12)相互作用来促进血管生成。研究人员通过Co-IP实验证实AGGF1与TNFSF12存在明确的相互作用。同时TNFSF12与成纤维细胞生长因子诱导型14(Fn14)结合,形成同源三聚体以促进血管生成。进一步研究发现AGGF1不与Fn14直接作用,但是AGGF1促进TNFSF12与Fn14的结合以增加血管生成。通过玻璃体腔注射抗AGGF1抗体可以有效抑制OIR模型中的病理性新生血管形成,并且与抗TNFSF12或抗VEGF治疗具有协同作用。这为缺血性视网膜病变的治疗提供了新的选择。

图3. 靶向AGGF1治疗改善视网膜病理性新生血管形成
注:玻璃体腔注射anti-IgG、anti-AGGF1、anti-TNFSF12、anti-AGGF1+TNFSF12、anti-VEGF、anti-AGGF1+VEGF的 OIR 小鼠全视网膜FITC染色代表图
04AGGF1通过上调增殖相关指标促进血管生成
为深入理解AGGF1调节血管生成的作用机制,研究人员通过蛋白组学分析和Western blot检测发现,在高糖处理的人视网膜微血管内皮细胞(HRMECs)中,AGGF1的沉默显著降低了细胞周期蛋白CyclinA2、CyclinD1和CDK1的表达。此外,AGGF1沉默的HRMECs在细胞增殖、迁移和成管能力方面均显著降低。这些结果都表明,AGGF1可能通过上调细胞周期蛋白的表达,促进内皮细胞的增殖和迁移,从而促进血管生成。
05SGLT2i抑制AGGF1表达进而延缓视网膜病变进展
内皮细胞AGGF1缺失促进缺血视网膜中健康的视网膜血管生成和异常血管消退。研究人员进一步研究钠-葡萄糖协同转运蛋白2抑制剂(SGLT2i)对视网膜的有益影响。在体内和体外观察了SGLT2i给药后的变化。结果发现给药后AGGF1表达明显降低,并抑制细胞周期通路的激活。提示SGLT2i通过抑制AGGF1信号通路实现了治疗效果,意味着AGGF1耗竭可能是预防缺血性视网膜血管病变恶化的一种有前途的治疗策略。
总结
本文发现AGGF1在缺血性视网膜病变患者中表达升高并诱导视网膜病理性新生血管形成,靶向AGGF1治疗可以改善视网膜病理性新生血管形成。该研究揭示了内皮AGGF1依赖性视网膜病理性新生血管形成的潜在机制,并提供了一种有效治疗缺血性视网膜病变的新思路。
天津医科大学朱宪彝纪念医院简介
天津医科大学朱宪彝纪念医院(代谢病医院),是以代谢性疾病诊治为特色的三级甲等综合性大学医院,以防治内分泌与代谢性疾病为特色。目前门诊年就诊量约 100 万人次,年住院人数超过2万人次,承担着天津市及周边地区广大疑难糖尿病患者的诊治工作,同时也肩负着提升区域整体糖尿病防治水平的重任。
天津市内分泌研究所是由国内外享有盛名的内分泌学家、天津医学院首任院长朱宪彝教授于1978年亲手创建,是中国内分泌领域第一个专业研究机构。2004年,天津市内分泌研究所与天津医科大学代谢病医院(现朱宪彝纪念医院)合并,实行院所合一的运行体制。天津医科大学朱宪彝纪念医院(代谢病医院) &天津市内分泌研究所,系国家“211 工程”重点建设学科—内分泌与代谢病专业,拥有国家卫生健康委员会激素与发育重点实验室、天津市代谢性疾病重点实验室、天津市国际联合研究中心以及天津市糖尿病防治国际科技合作基地等科研基地。院所致力于探索内分泌与代谢病性疾病发生和发展的关键分子机制,并进行疾病防控和转化医学研究。

专家简介

陈莉明教授
天津医科大学朱宪彝纪念医院
主任医师、博士生导师,天津医科大学朱宪彝纪念医院党委书记、院长,天津市内分泌与代谢重点实验室主任,IDF-WPR执委,CDS学会副主任委员,天津糖尿病学分会主任委员,国务院政府特殊津贴专家,国家卫健委中青年突出贡献专家,海河医学学者,天津名医,天津市优秀科技工作者,天津市高校 “学科领军人才”,《国际内分泌代谢杂志》主编、《中华糖尿病杂志》副主编。从事内分泌与代谢性疾病的临床和基础研究工作。主持国家级和省部级科研项目十五项。获得天津市科学技术进步二等奖、天津市技术发明二等奖、天津市教学成果特等奖等科技奖励。主持完成《中国血糖监测临床应用指南》等多个指南与共识,以第一/通讯作者身份发表SCI论文91篇。
原文链接:https://www.nature.com/articles/s41467-025-55970-3
