 文|近史演绎编辑|近史演绎
文|近史演绎编辑|近史演绎本研究为MRI诊断环境下的生物医学和治疗设备研制了新型MRI兼容的超低磁化率锆钌合金。结果表明,与钌合金化成纯锆将显著提高钌的强度和硬度性能。锆钌合金的耐蚀性显著提高。
用锆钌合金培养MG 63成骨细胞样细胞和L-929成纤维细胞时,可以发现高细胞活力并观察到健康的细胞形态,而锆钌合金的溶血率为<1%,远低于5%,根据ISO 10993-4标准生物材料的安全值。
与传统的生物医用316L不锈钢、Co-Cr合金和Ti基合金相比,锆钌合金的磁化率(1.25×10−6厘米3·g−1–1.29 × 10−6厘米3·g−1对于锆钌合金)是超低的,约为钛基合金(Ti-6Al-4V,~3.5 × 10)的三分之一−6厘米3·g−1, CP Ti 和 Ti–6Al–7Nb, ~3.0 × 10−6厘米3·g−1)和Co-Cr合金的六分之一(Co-Cr-Mo,~7.7 × 10−6厘米3·g−1).在Zr-Ru合金系列中,Zr-1Ru表现出增强的机械性能,优异的耐腐蚀性和细胞活力以及最低的磁化率,因此是MRI诊断环境下作为治疗设备的最佳Zr-Ru合金系统。
生物医用金属合金是生物医学材料和治疗设备领域非常重要的成员。据报道,超过70%的生物医学植入物和设备由金属生物材料制成,过去几十年中最常用的金属生物材料包括不锈钢(316L SS,304 SS),钴(Co)-铬(Cr)合金和钛(Ti)及其合金。
然而,据报道,这些具有高磁化率的传统金属生物材料会对磁共振成像(MRI)和诊断产生不利影响,因为它们会在MRI和诊断仪器的强磁场中被磁化,导致生物医学材料和治疗设备产生热量,生物医学材料和治疗设备位移以及MRI和诊断上的伪影。
这种伪影会扭曲植入物周围人体器官和组织的真实生物成像和诊断,从而妨碍准确的诊断。受伪影影响的区域与植入物的高磁化率有关,并且会随着磁化率的降低而减少,考虑到MRI的兼容性,在MRI下进行手术和诊断需要具有超低磁化率的材料和设备。

钌(Ru)属于铂族,具有超低磁化率,类似于合金元素Nb,Mo,Rh,Pd和Ag,Ru属于元素周期表中的4d过渡金属,Ru在潜在的生物医学应用中非常有前途,因为它们具有极强的生物相容性,在体外表现出低离子细胞毒性,在体内具有出色的生物相容性,没有致突变性或致癌性的证据,良好的耐腐蚀性和骨相容性等于或超过传统的纯Ti和Ti基生物医学材料。
众所周知,Ru 可将生物医用钛基合金的耐腐蚀性提高几个数量级,甚至添加 0.1% 的 Ru,并且已被广泛报道被纳入生物医学钛基合金中,先前的研究表明,在Zr基合金中添加Ru可以进一步提高显微硬度和耐磨性,根据Zr-Ru二元相图,表明Ru在Zr基质中的溶解度分别为12 wt.%(β相)和1 wt.%(α相)。当超过溶解度时,RuZr金属间化合物会分离出来。

本研究设计并制备了不同Ru合金元素含量的Zr-Ru合金,用于新型生物医用Zr合金,具有超低磁化率、增强的力学性能、改进的耐腐蚀性、优异的生物相容性和MRI相容性。此外,铸造合金还经过冷变形和退火处理,以进一步改变Zr-Ru合金的机械性能和耐腐蚀性。
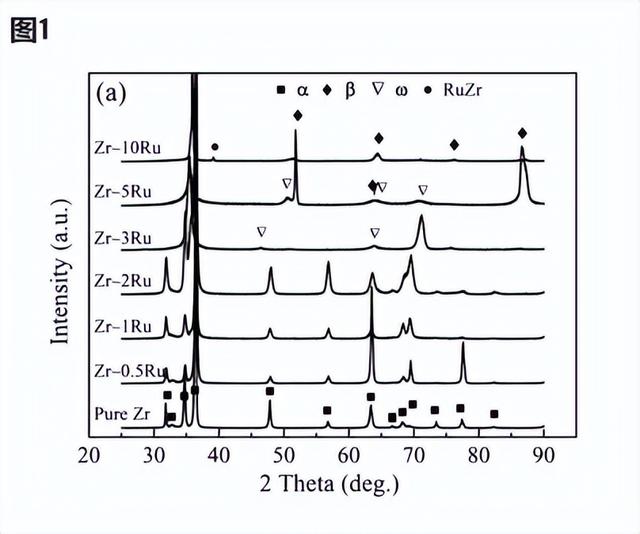
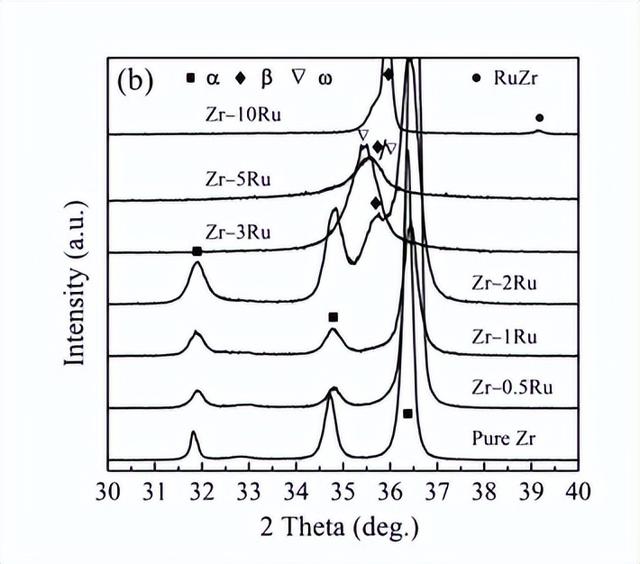
对于铸造的Zr-Ru二元合金,从图1可以看出,与纯锆相似,Zr-0.5Ru、Zr-1Ru和Zr-2Ru合金表现出单一的六边形紧密堆积结构(α相)。随着Ru含量的增加,Zr–3Ru、Zr–5Ru和Zr–10Ru合金的XRD图谱中出现了ω和β相。此外,在Zr-10Ru合金中观察到RuZr相。在冷加工至厚度减少50%并在600°C退火后,Zr-Ru合金发生了再结晶,如Zr-3Ru和Zr-5Ru合金中α相的重新出现和亚稳ω相的消失所示。

图2显示了铸造(a,b)和退火(c,d)纯Zr和Zr-Ru合金的拉伸应力-应变曲线(a,c)和拉伸力学性能数据(b,d)。可以看出,Zr-Ru合金的屈服强度(YS)和极限抗拉强度(UTS)均高于纯Zr,但铸造Zr-10Ru合金的屈服强度(YS)和极限抗拉强度(UTS)均高于纯Zr,但铸造Zr-10Ru合金在拉伸试验中表现出脆性断裂,伸长率最低,为1.4%。再结晶退火后, 纯Zr和Zr–Ru合金表现出更高的延展性, 因为它们的平均断裂伸长率超过10%.
图3显示了铸造(图3A)和退火(图3B)纯Zr和Zr-Ru合金的断裂显微照片。断裂形貌特征明显与拉伸实验结果一致。对于铸造组,纯Zr、Zr–0.5Ru和Zr–1Ru的断裂形貌表现出典型的韧性断裂,观察到许多凹陷模式。Zr-2Ru合金的酒窝非常小且浅,表明韧性下降。随着Ru含量的进一步增加,Zr-3Ru、Zr-5Ru和Zr-10Ru合金表现出典型的解理断裂,表明其韧性相对较差。退火后, 所有Zr-Ru合金均表现出典型的韧性断裂, 并观察到许多凹陷图案.

图4显示了铸造(a)和退火(b)纯Zr和Zr-Ru合金的显微硬度。可以看出,加入合金元素Ru后,Zr的显微硬度明显增强。铸造(a)和退火(b)合金的趋势都与相应的拉伸测试结果一致。对于铸造合金,趋势是抛物线型,Zr-3Ru合金具有最高的显微硬度(493 kg / mm2).对于退火合金,趋势是单调性上升,这导致Zr-5Ru合金具有最高的显微硬度。
图5展示了Hank溶液中退火纯Zr和Zr-Ru合金的电化学测试。根据开路电位(OCP)曲线(图5(a))和动电位极化曲线(图5(b)),以下参数包括OCP、腐蚀电位(E科尔)、腐蚀电流密度(i科尔)和击穿电位(E陈)可以计算,在Hank溶液中暴露2 h时,OCPs缓慢地向惰性电位变化,并达到相对稳定的纯Zr和Zr-Ru合金值。

OCP的持续增加意味着钝化膜在金属表面上自发形成。通过比较OCP值(补充信息S2),与Ru合金化后,这些合金的OCP比纯Zr增加,这表明Ru的添加使自发钝化膜在热力学上更稳定,从而使这些Zr-Ru合金比纯Zr具有更高的耐腐蚀性。在发生跨钝化之前,在偏振曲线的阳极分支上观察到一个钝化区域,表明钝化膜(氧化物)的增厚和生长。
结果表明, 目前Zr-Ru合金的稳定性均匀低于纯Zr, 这表明合金化提高了纯Zr的钝化性, 显示出更好的抗溶解保护.在更正电位时,被动薄膜分解,电流密度迅速增加。在补充信息S2中可以发现,与纯Zr相比,所有实验性Zr-Ru合金的腐蚀电流密度较低,这进一步表明Ru合金的添加提高了纯Zr的耐腐蚀性。此外,击穿电位(E陈)的Zr-Ru合金远高于纯Zr,进一步表明添加Ru合金元素增强了点蚀性能。

通过XPS分析检测了腐蚀试验前后Zr-Ru合金的元素分布,结果列在补充信息S3和S4中。XPS分析表明,Zr-Ru合金腐蚀表面的主要成分是ZrO2和若奥2而随着Ru含量的增加,RuO含量也越来越高增加。可以观察到,随着氧化钌与氧化锆比例的增加,耐腐蚀性增加。
图6显示了在不同时间段内在纯Zr和Zr-Ru合金的萃取介质中培养后的L929和MG63增殖。可见,培养1、3、5 d后,纯Zr和Zr–Ru合金的细胞活力与阴性组几乎相同,统计分析表明阴性对照、纯Zr和Zr–1Ru合金组间差异无统计学意义(p > 0.05)。此外,纯Zr和Zr-Ru合金基团的细胞形态与阴性对照组相似,即健康,扩散和拉伸良好,可以观察到纺锤形或细胞多边形,会聚和laminipodia。

图7显示了纯Zr和Zr-Ru合金的溶血率。纯Zr和Zr-Ru合金的溶血率相当低(小于1%),远低于5%,根据ISO 10993-4标准对生物材料的安全值,表明纯Zr和Zr-Ru合金在与血液接触时不会对红细胞或溶血造成破坏性影响。

纯Zr在室温下与外加磁场的磁化变化如图8(a)所示。与纯Zr类似,Zr-Ru合金在磁化强度和外加磁场之间表现出均匀的线性变化关系,因此此处省略了曲线。取而代之的是,纯Zr和Zr-Ru合金的磁化率由通过数据的线性拟合的斜率确定,绘制在图8(b)中。显然,加入合金元素Ru后,磁化率明显下降。最有效的组成点在于1%的Ru添加,磁化率最低,为1.247×10−6厘米3·g−1,表明与纯Zr相比,MRI兼容性要好得多(磁化率为1.475×10−6厘米3·g−1).

在我们最近的工作中,使用二元Zr-1X(X = Ti,Nb,Mo,Cu,Au,Pd,Ag,Ru,Hf和Bi)合金模型筛选出具有优异生物相容性和MRI相容性的Zr的最佳合金元素,发现元素Ru是最有效的元素。在本工作中,我们尝试使用具有各种Ru含量(0.5重量%,1重量,2重量%,3重量%,5重量%和10重量%)的Zr-Ru二元合金模型来优化元素Ru的最佳添加含量。

出于机械性能考虑,Zr-Ru合金的Ru含量应低于2%wt.;随着Ru合金元素的添加,与纯Zr相比,Zr-Ru合金的强度和硬度均显著提高。但对于含有较高Ru含量(高于2 %wt.)的Zr-Ru合金,观察到伸长率显着降低,这可能是由于ω相和RuZr沉淀物的出现,这通常会对生物医用合金作为生物相容性和治疗装置的延展性和韧性产生破坏性影响。

出于耐腐蚀性的考虑,Ru含量(0.5~5%重量)的Zr-Ru合金优于纯Zr;当将Ru元素合金化时,Zr的耐蚀性显著提高,这可以通过腐蚀电位(E科尔)和击穿电位(E陈)在无Ru纯Zr对照组上向贵向移动。目前的结果表明,Ru添加可以赋予Zr基合金更大的耐腐蚀性,降低合金作为阳极位点的倾向和电压高达+1.1 V高于E时的瞬态电流科尔,支持Ru添加到Zr基合金中提高耐腐蚀性的能力。

从细胞相容性和血液相容性考虑,Ru含量(0.5~5% wt.)的Zr-Ru合金与纯Zr一样好;与合金元素Nb,Mo,Rh,Pd和Ag相似,元素Zr和Ru都属于元素周期表中的4d过渡金属,它们具有极强的生物相容性,在体外表现出低离子细胞毒性,在体内具有出色的生物相容性,没有致突变性或致癌性的证据以及骨相容性等于或超过传统的纯Ti和Ti基生物医学材料和治疗设备。

出于MRI相容性的考虑,Ru含量为1% wt.的Zr-Ru合金磁化率值最低;众所周知,MRI是一种非侵入性诊断工具,不会对患者进行电离辐射,并且避免使用肾毒性造影剂。然而,在高强度的磁场下,具有高磁化率(χ)的顺磁性金属,如生物医学316L不锈钢、Co-Cr合金和Ti基合金,会因磁场失真而在图像中产生伪影。

因此,为了减少伪影并获得真实的诊断MRI成像,开发具有超低磁化率的新型金属植入物,从而具有更好的MRI兼容性具有相当大的兴趣。本工作证明Zr-Ru合金的超低磁化率(1.25 × 10−6厘米3·g−1–1.29 × 10−6厘米3·g−1对于Zr-Ru合金)仅为Ti基合金(Ti-6Al-4V,~3.5×10)的三分之一−6厘米3·g−1, CP Ti 和 Ti–6Al–7Nb, ~3.0 × 10−6厘米3·g−1)和Co-Cr合金的六分之一(Co-Cr-Mo,~7.7 × 10−6厘米3·g−1)19,这是众所周知的普遍广泛用于生物医学材料和具有高磁化率的治疗设备,不适用于MRI诊断。

众所周知,在目前的临床治疗和操作中,特别是对于微创手术和疗法,某些介入医疗植入物和装置,如导管、过滤器、导丝器、支架移植物、针头等,可能需要MRI程序来确定设备的位置,并在用MRI技术查看的过程中输送药物。在Zr-Ru合金系列中,Zr-1Ru表现出增强的机械性能,优异的耐腐蚀性和细胞活力以及最低的磁化率,因此是上述生物医学材料和治疗设备在MRI技术和诊断环境下使用的最佳Zr-Ru合金体系。
