在化学领域中,浓硫酸广为人知,但还有比它更强的酸。你可知有一种酸,让浓硫酸在其面前如同柠檬汁般毫无“杀伤力”,你知道是哪种酸吗?
谈及化学中最具危险性和破坏力的物质,很多人会首先想到酸。在影视作品中,如《绝命毒师》里老白用酸溶人,《蝙蝠侠》中小丑因酸毁容而走上反派之路,可见在人们印象中,反派使用酸作武器时,显得强大而恐怖,相比之下碱则温和许多。
那么,哪种酸才是酸中的王者呢?下面来盘点酸类战力排行榜的前三名。
01
弱酸
日常生活中,酸无处不在。
人体每天会产生尿酸,5克纯尿酸约是一人10天的排泄量,饱和尿酸溶液pH值约4.6,可见尿酸是弱酸。
可乐中含碳酸,饱和碳酸pH值仅3.7,实际测量可乐pH值约2,因其中还含磷酸。

牛奶倒入可乐中会发生剧烈反应,就是磷酸与牛奶中物质相互作用的结果,而1摩尔每升磷酸的pH值约为1.1,磷酸也是弱酸。
说到强酸,氢氟酸名气大,腐蚀性强能溶玻璃,容器都难盛放,且滴到手上会渗入皮肤,剧毒无比,但1摩尔每升氢氟酸的pH值约1.6,属弱酸。
尿酸、碳酸、磷酸、氢氟酸等溶于水后只能部分电离氢离子,属弱酸范畴,水中能完全电离的才是强酸。
02
强酸
世界公认的三大强酸是盐酸、硝酸、硫酸,它们在初中化学酸类物质中酸性极强。

初中学习化学时,若给这三种强酸排名,盐酸具刺鼻易挥发特性,硝酸强调氧化性和腐蚀性强,硫酸则比它们多一个氢。
能否通过pH值确定最强酸呢?答案是否定的,因水中存在拉平效应,三种完全电离的强酸在水中酸性表现一样强,如1摩尔每升的盐酸和硝酸pH值均为0。
后来化学家提出pKa概念,它是酸解离方程平衡常数的负对数,可衡量酸解离氢离子的绝对能力,更客观地比较酸的强弱。pKa值越小酸性越强,且每相差1,酸性相差10倍。
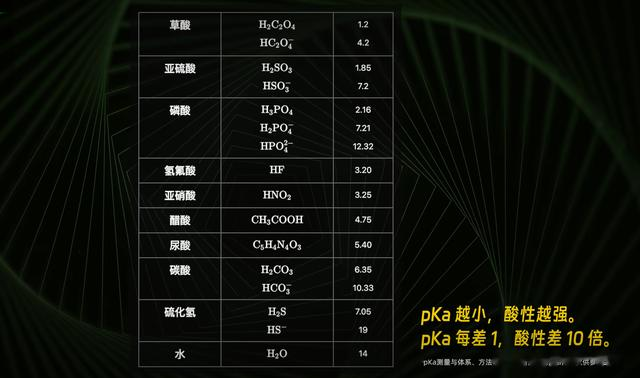
借助此评价体系,硝酸pKa值为-1.3,硫酸pKa值为-3,盐酸pKa值为-7,可见硝酸相对较弱,硫酸并非最强,盐酸才是三大强酸中的“老大”。
此外,王水由浓硝酸和浓盐酸按1:3比例混合而成,能溶解黄金,硝酸强氧化,盐酸氯离子强配位,但王水不稳定,需现配现用,酸性只是普通强酸水平。
食人鱼洗液由硫酸和双氧水混合,氧化腐蚀性强,能“吞噬”许多物质,但酸性也未超出强酸范畴。
盐酸虽是初中常见酸中的最强者,但并非酸中的终极强者,氢碘酸是氢卤酸中的“强者”。
03
超酸
强酸之上还有超酸,其定义是比100%硫酸酸性更强的酸。1887年阿伦尼乌斯提出酸的水溶液电离定义,1923年布朗斯特和劳里提出酸碱质子理论,从广义说,超酸是极易给出氢离子的物质,纯硫酸在超酸面前也会接受氢离子。

因超酸酸性过强,离子活度变化使测量pKa值的假设不适用,化学家又定义了哈米特函数(H0),H0值越小酸性越强,H0值每小1,酸度强10倍。纯硫酸H0值为-11.9,而纯硫酸之上至少有11种更强的超酸。
2004年,科学家合成出最强单一分子酸——碳硼烷酸,熔点高,H0值难以准确测定,保守估计低于-18,酸性比纯硫酸强100万倍,其稳定的碳硼烷酸根使其酸性超强,暂排第三。
氟硫酸和五氟化锑混合得到的魔酸,H0值达-23,比纯硫酸强1000亿倍。1966年,因学生将蜡烛置入魔酸中迅速溶解这一现象,该酸遂被命名,欧拉教授也因此荣获1994年诺贝尔化学奖。
世界上最强的酸是氟锑酸,H0值达-28,酸性比纯硫酸强1亿倍。将其滴在鸡腿上,瓶子打开就冒烟,65%的氟锑酸溶液威力就很大。如此强的酸需用特氟龙等特殊材质容器盛放。

对很多人来说,追求最强酸似显“中二”,但化学家追求酸性战力极限,是源于对未知的探索和科学边界的挑战,源自人性的好奇心,渴望了解化学边界,借助更强酸创造新分子、催化化学反应。
1925年发现的氦氢离子是已知最强酸,有人推测它的H0值达-63,可能代表宇宙中第一个化学键。在氦氢之后,人类或许还会找到更强的酸,好奇心正是推动科学进步的原动力。
【文本来源@毕导的视频内容】
