
非小细胞肺癌(NSCLC)在肺癌中约占80%~85%[1],绝大多数患者确诊时已属晚期[2]。尽管免疫治疗和靶向治疗改善了晚期NSCLC的预后,但疾病进展仍不可避免。就晚期NSCLC二线及后线治疗而言,目前治疗方案的临床获益有限且往往有较大的耐受性问题,因此亟需更为有效、安全性更好的治疗选择,以延长患者生存获益和改善生活质量[2]。
Datopotamab deruxtecan(Dato-DXd)是一种新型的靶向滋养细胞表面抗原2(TROP2)的抗体偶联药物(ADC),由人源化的抗TROP2免疫球蛋白G1单克隆抗体与有效载荷强效拓扑异构酶I抑制剂通过稳定的、具有肿瘤选择性的、基于四肽的可裂解连接子偶联而成[2]。之前,TROPION-PanTumor01研究的NSCLC队列数据已多次在各大国际学术会议如美国临床肿瘤学会(ASCO)年会、世界肺癌大会(WCLC)、欧洲肿瘤内科学会(ESMO)年会上进行结果更新,研究结果显示,Dato-DXd治疗晚期NSCLC可带来有前景的疗效获益。
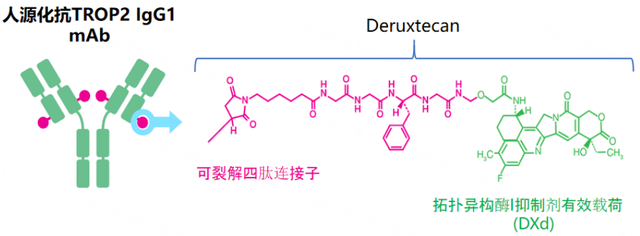
图1. Dato-DXd结构示意图
近日,国际肿瘤著名期刊《临床肿瘤学杂志》(Journal of Clinical Oncology,影响因子50.717)发表了TROPION-PanTumor01研究NSCLC队列的更新结果全文,进一步证实了Dato-DXd在经治晚期NSCLC患者具有令人鼓舞的抗肿瘤活性和可控的安全性[2]。
TROPION-PanTumor01研究:Dato-DXd用于经治晚期NSCLC安全性可控、疗效显著
纳入晚期NSCLC人群,进行疗效分析TROPION-PanTumor01是一项在实体瘤(包括晚期NSCLC)患者中,评估Dato-DXd治疗安全性、耐受性和抗肿瘤活性的多中心、开放标签、Ⅰ期、两阶段(剂量递增和剂量扩展)、首次人体研究。

图2. TROPION-PanTumor01 NSCLC队列的研究设计
在NSCLC队列,纳入了年龄≥18岁(美国)或≥20岁(日本)、美国东部肿瘤协作组(ECOG)体能状况(PS)评分0~1分、经标准治疗后复发/进展(或没有标准治疗可用)的晚期/转移性NSCLC有或无可靶向基因组改变(AGA)的患者。在剂量递增阶段,患者接受0.27~10 mg/kg Dato-DXd,每三周一次(Q3W);在剂量扩展阶段,患者接受4、6或8 mg/kg Dato-DXd Q3W。主要终点是安全性和耐受性。次要终点包括客观缓解率(ORR)、生存和药代动力学。
在跨研究阶段接受Dato-DXd 4~8 mg/kg的患者中,基线时有54%~64%的患者既往接受了≥3线治疗,20%~24%患者既往接受了≥5线治疗,76%~88%患者既往接受过免疫治疗,96%~98%患者既往接受过基于铂类化疗;30例携带EGFR突变(15例为19号外显子缺失,12例为T790M突变,3例为20号外显子插入),3例携带ALK融合,1例携带ROS1融合,1例携带RET融合(表1)。在35例AGA患者中,共有69%既往接受过奥希替尼治疗。
表1. NSCLC队列跨研究阶段接受4-8mg/kg患者的基线特征

更新结果显示,210例患者接受了Dato-DXd治疗。其中,180例在剂量递增阶段及剂量扩展阶段接受了Dato-DXd 4~8 mg/kg Q3W(4 mg/kg,50例;6 mg/kg,50例;8 mg/kg,80例)。接受4、6和8 mg/kg患者的中位研究持续时间分别为15.9个月、13.3个月和20.6个月,中位暴露时间分别为4.1个月、3.5个月和3.3个月[2]。
推荐剂量6 mg/kg展现出高度鼓舞的抗肿瘤活性,ORR 26%、中位PFS 6.9个月、中位OS 11.4个月Dato-DXd 4、6、8 mg/kg剂量均显示了抗肿瘤活性(表3和图3)。接受Dato-DXd 4、6、8 mg/kg患者的确认ORR分别为22%、26%、23.8%,疾病控制率(DCR)分别为76.0%、70.0%、78.8%,中位缓解持续时间(DOR)分别为12.7个月、10.5个月、9.6个月,中位无进展生存(PFS)分别为4.3个月、6.9个月、5.2个月,中位总生存(OS)分别为12.9个月、11.4个月、10.5个月。同时,无论TROP2表达水平如何,患者对Dato-DXd治疗均有应答。
本次分析也显示,与4或8 mg/kg剂量组相比,6 mg/kg剂量组的疗效更好或与之相当[2]。6 mg/kg Q3W用于进一步研究或探索的推荐剂量。
表2. NSCLC队列疗效


图3. NSCLC队列的Dato-DXd抗肿瘤活性。(A)根据RECIST 1.1,靶病变直径总和相对于基线的最大百分比变化,Dato-DXd 4、6或8 mg/kg以不同颜色条形图表示;(B)Dato-DXd 6 mg/kg剂量组患者靶病变大小随时间变化的情况,有应答者和无应答者用不同颜色的线形图表示。

图4. 在NSCLC队列中接受Dato-DXd 6mg/kg患者的Kaplan-Meier生存曲线。(A)盲态独立中心审查评估的无进展生存(PFS);(B)总生存(OS)。
安全性可控,血液学毒性、腹泻等发生率低Dato-DXd治疗的最大耐受剂量为8 mg/kg Q3W,相比之下,6 mg/kg剂量表现出了更好的耐受性。最常见的任何级别治疗期间出现的不良事件(TEAE)为恶心、口腔炎和脱发(表4)。最常见的≥3级TEAE为肺炎、贫血和淋巴细胞计数减少。
值得注意的是,目前晚期NSCLC的二线或后线标准治疗(SOC)即多西他赛联合或不联合血管内皮生长因子(VEGF)抑制剂,与较高的中性粒细胞减少症(14%~67%)、发热性中性粒细胞减少症(2%~16%)、腹泻(2%~42%)、TRAE导致死亡(0%~16%)发生率相关。然而,Dato-DXd治疗的血液学毒性轻微,任何级别中性粒细胞计数减少(包括中性粒细胞减少症)的发生率为5.6%,且大多数中性粒细胞减少症为1或2级,没有≥4级的中性粒细胞减少症或任何级别的发热性中性粒细胞减少症;腹泻率低(Dato-DXd 4 mg/kg组为10.0%,6 mg/kg组为18.0%,8 mg/kg组为18.8%),且无≥3级腹泻[2]。
表3. 发生率≥15%的TEAE及间质性肺疾病(ILD)发生情况

鉴于Dato-DXd的独特ADC特征及其在晚期NSCLC中展现的良好治疗效果,支持进一步研究Dato-DXd用于NSCLC的效果。在针对晚期NSCLC开展的Ⅲ期研究中,TROPION-Lung01旨在评估Dato-DXd单药用于经治晚期NSCLC有或无AGA患者的效果,结果即将在学术大会上公布,非常令人期待;另外,还包括针对晚期一线TROPION-Lung08(在PD-L1≥50%人群中使用Dato-DXd+帕博利珠单抗对比帕博利珠单抗)、TROPION-Lung07(在PD-L1<50%人群中使用Dato-DXd+帕博利珠单抗±铂类化疗对比博利珠单抗+铂类化疗)和AVANZAR(Dato-DXd+度伐利尤单抗+卡铂对比帕博利珠单抗+铂类化疗),其结果同样值得期待。
王哲海教授点评
ADC有“魔法子弹”的美誉,其将靶向治疗的精准性和化疗药物的强效毒性作用“集于一身”,是晚期NSCLC领域的重大突破。
ADC药物Dato-DXd的TROPION-PanTumor01全文公布,则为晚期经治NSCLC患者带来了新的潜在治疗选择。与现有晚期NSCLC二线SOC的研究相比,TROPION-PanTumor01研究中NSCLC队列的患者接受的既往治疗线数更多(>50%的患者接受过≥三线治疗,21.7%的患者接受过≥五线治疗),且不论是否有驱动基因改变, Dato-DXd均展现了很好的疗效。其中Dato-DXd 6mg/kg治疗的ORR为26%,DCR为70.0%,中位DOR为10.5个月,中位PFS为6.9个月,且安全性可耐受[2],这非常令人振奋,为后续进一步研究和探索奠定了基础。
据悉,针对晚期2L+治疗的Ⅲ期注册研究TROPION-Lung01研究旨在评估比较Dato-DXd 6 mg/kg与多西他赛治疗经治晚期或转移性NSCLC(有或无AGA)患者的效果,已经公布了主要研究终点之一PFS达到了阳性结果,详细数据将在近期国际大会上公布,有望成为肺癌领域首个报道关键研究结果的TROP2-ADC药物Ⅲ期临床试验,为晚期NSCLC患者提供一种全新的有效治疗选择,我们拭目以待!
专家简介
王哲海 教授
山东第一医科大学附属肿瘤医院呼吸科,副院长、主任医师;
中国临床肿瘤学会常务理事;
中国临床肿瘤学会非小细胞肺癌专家委员会副主任委员;
中国临床肿瘤学会抗肿瘤药物安全专家委员会副主任委员;
中国医促会胸部肿瘤分会副主任委员;
中国初级医疗保健基金会肺癌专业委员会副主任委员;
山东抗癌协会常务理事;
山东省癌症中心副主任;
山东省抗癌协会肺癌分会主任委员
参考文献:
[1] 原发性肺癌诊疗指南(2022 年版).
[2]Shimizu T, Sands J, Yoh K, et al. First-in-Human, Phase I Dose-Escalation and Dose-Expansion Study of Trophoblast Cell-Surface Antigen 2-Directed Antibody-Drug Conjugate Datopotamab Deruxtecan in Non-Small-Cell Lung Cancer: TROPION-PanTumor01[J]. J Clin Oncol. Published online June 16, 2023.
* 此文仅用于向医学人士提供科学信息,不代表本平台观点

