*仅供医学专业人士阅读参考

抗体药物偶联物(ADC)是近年来肿瘤领域极具前景的一种新型治疗方式,ADC平台的概念是通过将细胞毒性药物选择性地递送至肿瘤细胞,并且限制暴露于健康的正常细胞,从而增加细胞毒性药物的治疗指数。尽管ADC相比传统化疗的靶向性大大增强,但是也不可避免报告正常细胞/组织中的剂量限制性毒性(DLT)。目前,DLT仍然是ADC开发的关键挑战。ADC在正常细胞/组织中的毒性机制尚不清楚,但认为大多数DLT与靶点无关。除了连接子-药物不稳定性导致循环中细胞毒性药物(有效载荷)过早释放外,受体依赖性(FcγR、FcRn和C型凝集素受体)和受体非依赖性(非特异性内吞)机制摄取/转运ADC可能导致正常细胞的脱靶毒性。发表在《Pharmacol Ther》上的一篇综述[1],回顾了正常细胞中ADC非靶点依赖性摄取和毒性的潜在机制,并讨论了可能影响这些机制的潜在原因。相关内容能为更加深入地了解ADC脱靶毒性的潜在机制提供依据,有助于开发规避这些机制的方法,进而改善下一代ADC的总体治疗指数。现将该综述中有关连接子-药物不稳定性、非特异性内吞作用的相关内容梳理如下,以飨读者。
ADC药物非靶点依赖性摄取和毒性的机制
尽管ADC毒性被认为主要来源于有效载荷,但非靶向正常细胞摄取ADC,并释放出有效载荷从而产生毒性的相关机制尚不清楚。这种摄取可通过多种机制发生,目前正在进行相关研究来了解这些机制并优化ADC的三种关键组分(即单克隆抗体、连接子和有效载荷)。根据大多数估计值,ADC在人体靶(肿瘤)部位仅发生适度的蓄积(每克肿瘤约0.1%的给药剂量)。因此,ADC的主要部分保留在循环中或分布到正常组织中,可能被摄取和分解代谢,导致正常细胞毒性。靶点依赖性和非依赖性摄取机制均可能造成正常细胞的ADC摄取和毒性。本综述将重点关注正常细胞对ADC非靶点依赖性摄取(也称为非特异性摄取)及其可能导致的脱靶毒性的机制等相关内容。
表1. ADC中使用的不同类别有效载荷的详细信息和临床研究中通常报告的主要毒性

1.连接子-药物不稳定性
连接子-药物不稳定性可导致有效载荷过早释放到血液中,并导致ADC的脱靶毒性。连接子的选择是ADC稳定性背后的主要驱动因素之一。第一代ADC药物采用酸可裂解连接子(例如,腙),其被设计为在血浆中性pH环境中稳定,但ADC内化后能在溶酶体内较低pH条件下释放。
然而,这些早期ADC往往受到血浆稳定性差的困扰,从而导致循环中有效载荷的脱落(图1)。导致ADC血浆不稳定性的因素包括对血清蛋白酶的敏感性,尤其是基于肽的连接子和自发去偶联,如逆转录酶-Michael马来酰亚胺转移到血浆蛋白上存在的游离巯基上。除安全性问题外,不稳定ADC的疗效也可能降低,因为到达肿瘤的ADC不再完整偶联有效载荷。在某些情况下,引入不可裂解连接子可缓解连接子裂解问题。比较具有可裂解连接子(SPP-DM1和mc-VC-PAB-MMAE)和不可裂解连接子(mcc-DM1和mc-MMAF)类型ADC的结果显示,对于特定靶标(CD22),具有不可裂解连接子的ADC的毒性(肝脏和血液学毒性)降低。同样,与含有可裂解二硫键的美登素类ADC相比,含不可裂解硫醚MCC连接子的ADC,其临床前安全性特征得到改善。采用不可裂解连接子ADC的毒性降低被认为是由于进入体循环的游离细胞毒性有效载荷释放减少。然而,并非所有靶抗原均适用于含不可裂解连接子的ADC的治疗,因为需要将完整的mAb分解代谢才能释放连接药物以发挥抗肿瘤作用。

图1. 正常细胞摄取ADC或游离有效载荷的潜在机制。靶抗原可能在正常细胞上表达,并有助于ADC的靶点依赖性摄取。此外,结合IgG抗体Fc保守区的其他受体,如Fcγ受体(FcγR)、新生儿Fc受体(FcRn) 和C型凝集素受体(CLR)也可能有助于正常细胞中ADC的非靶点依赖性内化/转运。非特异性内吞机制,如巨胞饮或小胞饮也可能导致完整ADC或游离有效载荷内化(由于连接子-药物不稳定或胞外蛋白酶活性在细胞外释放)。游离有效载荷也可能通过其他机制进入正常细胞,如被动扩散(如果具有膜渗透性)、非特异性内吞或特异性转运蛋白(如果膜转运蛋白的底物)介导的摄取。此外,抗原阳性靶细胞还能够通过将有效载荷释放到局部环境中介导毒性,随后被抗原阴性正常细胞(旁观者效应)通过被动扩散、转运蛋白介导的摄取或通过其他非特异性内吞机制摄取。
含可裂解连接子的ADC也可能通过旁观者效应增加疗效,是针对拷贝数较低、肿瘤表达异质性或内化率较低的肿瘤细胞靶抗原的首选。因此,连接子-药物稳定性仍然是未来ADC研发优化的关键领域,旨在最大限度地提高获得成功的ADC的概率。对于作用强效和具有膜渗透性的细胞毒素,如吡咯苯二氮卓类(PBD),关注含此类有效载荷的ADC的稳定性尤其重要。此外,除了连接子的可裂解性,释放有效载荷的膜渗透性同样可能影响正常细胞中潜在的脱靶细胞毒性,从而影响ADC的治疗指数。
结合位点也可能调节ADC的稳定性和药代动力学。使用表面暴露的氨基酸(如赖氨酸或半胱氨酸)的传统非特异性偶联方法会产生高度异质性的ADC(药物-抗体比[DAR],0-8),从而导致ADC的聚集机会增加,并且其整体血浆稳定性也会降低。因此,这些采用非特异性结合位点的ADC也可能导致正常细胞中非靶点依赖性摄取和毒性增加的安全性挑战。近年来,先进的连接子技术和对结合位点认识的提高产生了更多的均一性高的ADC,同时改善了总体连接子-药物的稳定性并减少了血浆中细胞毒性有效载荷的过早脱落。这些具有更高连接子-药物稳定性的ADC也可以发生更多由靶点驱动的有效载荷释放,从而提高疗效。因此,各种偶联位点工程策略,包括使用特定氨基酸(天然或工程)、Fc聚糖和短肽标签的几种特异性位点偶联,已被用于生成具有改善安全性特征的DAR均质性ADC。
例如,采用首个特异性位点偶联技术--THIOMAB(未配对半胱氨酸介导的偶联)偶联技术的ADC,其在临床前的耐受性相对优于具有相同有效载荷和非特异性偶联技术的传统ADC。此外,在临床前研究中,由半胱氨酸工程抗体和PBD(使用新型自燃二硫键连接子)组成的ADC显示出改善的安全性特征(降低毒性),且疗效相当,表明其可潜在增加ADC的治疗指数。
1.1 与连接子-药物不稳定性相关的ADC毒性中性粒细胞减少症(中性粒细胞计数降低)是ADC的一种重要的非靶点依赖性DLT,由于血浆中可裂解连接子不稳定,导致膜渗透性游离有效载荷提前释放。中性粒细胞减少是许多通过蛋白酶可裂解的缬氨酸-瓜氨酸(VC)连接子与MMAE结合而成的ADC的常见毒性,如Brentuximab vedotin、ASG-5ME、Glembatumumab vedotin、Indusatumab vedotin、Polatuzumab vedotin和PSMA ADC。Zhao等人[2]最近进行的一项体外机制研究表明,基于VC-MMAE的ADC诱导的中性粒细胞减少症是由于释放的有效载荷对骨髓中分化的中性粒细胞的直接细胞毒性作用所致。根据连接子化学,VC连接子预期在溶酶体中发生细胞内半胱氨酸蛋白酶介导的裂解。Zhao等人[2]的研究结果揭示,在骨髓微环境中局部分化的中性粒细胞分泌的丝氨酸蛋白酶有助于VC连接子在细胞外的切割,并释放膜渗透性MMAE导致对骨髓中分化的中性粒细胞的细胞毒性。然而,这项研究的结果提出了另一个问题,即为什么在骨髓细胞外释放的膜渗透性MMAE有效载荷仅对分化的中性粒细胞(髓系细胞)有毒性,而对骨髓中的其他多种敏感细胞类型如造血干/祖细胞、红系和巨核细胞系细胞没有毒性,因而这需要进一步研究论证,特别是使用体内模型比较基于可裂解和不可裂解连接子-MMAE的ADC的血液毒性(特别是分化骨髓细胞的毒性),以明确了解和证实细胞外丝氨酸蛋白酶在中性粒细胞减少症中的作用。
同样,周围神经病变(PN,周围神经损伤的结果)是另一种与微管抑制剂ADC(不考虑靶抗原)相关、导致治疗中止和/或剂量降低的重要非靶点依赖性临床毒性。PN被认为是由连接子-药物不稳定性驱动,从而导致体循环中膜渗透性游离有效载荷(微管抑制剂)过早释放所引起的毒性。微管抑制剂可破坏间期微管功能,这对于将关键必需蛋白从神经元胞体主动转运至远端突触至关重要,最终导致周围神经病变。
PN的特征为四肢麻木和刺痛,最终可能加重并导致极度疼痛和无力,通常在含膜渗透性MMAE有效载荷的ADC重复给药后观察到(与蛋白酶可裂解连接子连接,例如VC连接子),但不表现在含膜不可渗透有效载荷MMAF的ADC中。此外,PN是几乎所有含膜渗透性美登素(DM1和DM4)有效载荷与可裂解连接子结合的ADC的常见不良事件。
除了在体循环中被动扩散游离膜渗透性有效载荷外,ADC通过受体依赖性或非依赖性机制的分布/摄取也可能发生在周围神经中。因此,需要进行额外的体内调查研究,以明确了解周围神经的有效载荷/ADC暴露机制。值得注意的是,在临床前动物模型中并不总能预测临床中观察到的PN。例如,对基于VC-MMAE的ADC进行的标准临床前毒理学研究无法预测在临床中观察到的PN。然而,对于其他含微管抑制剂(如DM1或DM4)的非MMAE ADC,若在临床前种属中观察到PN,这种不良反应在临床表现中的可预测性良好。
1.2旁观者效应
除了靶抗原阳性细胞摄取ADC后的直接细胞毒性外,ADC的游离有效载荷也可能通过旁观者效应对邻近的靶抗原阴性细胞产生细胞毒性。在表达抗原的靶细胞(靶抗原阳性)中,ADC经内化进入肿瘤细胞后,随后在溶酶体中被分解代谢,并在细胞质中释放出游离有效载荷。然后游离有效载荷既可以被动扩散进入细胞外间隙(膜渗透性、高亲脂性有效载荷),也可以由于细胞膜完整性的丧失而被释放(靶细胞死亡后)。释放的游离有效载荷可能通过被动扩散、转运蛋白介导的摄取或通过其他非特异性内吞机制进入靶抗原阴性的正常细胞,从而引起细胞毒性。
ADC的旁观者效应通常与肿瘤杀伤(疗效)增加相关,尤其是针对抗原表达异质性的肿瘤。使用体外菌落球体试验和共培养系统以及体内异种移植模型证明了旁观者效应对于ADC效力和有效性的影响。然而,达到旁观者效应所需的细胞膜渗透性增加也可能导致脱靶毒性。因而与采用不可裂解连接子、不可渗透有效载荷的ADC相比,释放的膜渗透性有效载荷可能渗入正常组织,并导致毒性增加。例如,Cantuzumab mertansine(Can-M)和Cantuzumab ravtansine(Can-R)是靶向CanAg(肿瘤相关碳水化合物抗原,MUC1的一种新型糖型)的两种ADC,但分别具有相对不稳定的SPP[N-琥珀酰亚胺基4-(2-吡啶基二硫代)戊酸酯]连接子/DM1和稳定的SPDB(N-琥珀酰亚胺基-4-(2-吡啶基二硫代)丁酸酯)连接子/DM4的连接子/有效载荷组合。然而,仅在接受Can-M治疗的实体瘤肝转移患者中,观察到肝毒性(转氨酶升高),表明是由于ADC对邻近正常肝细胞的旁观者效应所致[3]。ADC技术的最新进展带来了细胞毒性有效载荷的发展,其可在肿瘤细胞中代谢为膜不可渗透性代谢物(例如,Dolaflexin)(Hofland,2016)。这种方法可能控制旁观者效应带来的不良影响--既保留杀死肿瘤细胞的有益化学性质,同时也显著降低针对正常细胞的全身毒性。
2.非特异性内吞作用
内吞作用是细胞摄取营养物质、调节跨膜动力学和突触囊泡再循环等的基本过程。内吞作用也可在大分子(包括IgG/ADC)摄取和分布至正常细胞中发挥重要作用。内吞作用大致分为吞噬作用(颗粒内化)和胞饮作用(可溶性分子内化,也称为液相内吞作用)。此外,根据内吞囊泡形成的大小,内吞作用已被分为大尺度和微尺度内吞过程。然而,在不同的已发表参考文献中使用的内吞机制的不同命名中观察到部分重叠概念并不少见。可能导致IgG/ADC非特异性摄取的主要内吞机制的关键特征列于下表。
表2. 主要内吞机制的关键特征

大尺度内吞作用包括吞噬作用和巨胞饮作用,分别涉及大颗粒或大体积部分的内化。吞噬作用涉及将大规模颗粒摄取到包围颗粒的细胞膜变形(肌动蛋白的局部重排)中。含有ADC或ADC聚集体的免疫复合物也可能被该过程摄取。与吞噬作用相似,巨胞饮也是一种肌动蛋白依赖性过程,它涉及在相对大量的细胞外液(而不是颗粒)区域周围形成质膜的皱褶延伸,以介导内吞作用。微尺度的内吞过程涉及使用大小小于200nm的微粒体吞噬较小体积物质。这些过程往往需要像网格蛋白或小窝蛋白这样的特殊外壳蛋白(图2)。Clathrin介导的内吞作用(CME)是大多数细胞类型中受体介导的微尺度内吞作用的主要形式,也是ADC靶向内化进入靶抗原/受体表达细胞的主要机制。配体与特定膜受体的结合启动了信号事件的级联反应,导致募集特定的接头蛋白进行网格蛋白包被的囊泡形成(图2),这些新形成的囊泡被动力蛋白(GTP酶)切断,并释放用于进一步的细胞内转运。小窝蛋白介导的内吞作用涉及膜包被蛋白小窝蛋白形成的烧瓶状结构(小窝),它也依赖于动力蛋白进行囊泡分裂。小窝蛋白介导的摄取在许多细胞类型中起主要转运作用,尤其是在内皮细胞中占优势。重要的是要认识到,除网格蛋白和小窝蛋白介导的内吞作用外,还存在其他几种微吞过程,包括CLIC/GEEC、ARF6、Flotillin和四跨膜蛋白相关过程。
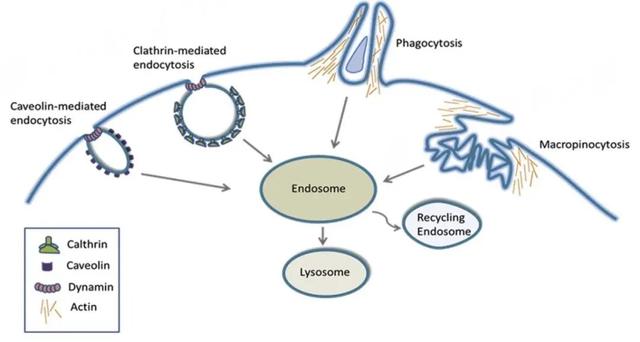
图2. 宏观和微观内吞过程的关键结构特征示意图。吞噬作用涉及FcγR结合Cdc42(细胞分裂周期蛋白42)和Rac1(Ras相关C3肉毒毒素底物)的局部激活导致肌动蛋白聚合。巨胞饮过程涉及大量液体的摄取,形态学特征为皱褶的巨胞饮小体。小窝内吞作用的特征是通过电子显微镜(EM)可见与胆固醇相关的小窝的尖峰样包被。最明确的微尺度内吞过程包括网格蛋白介导的内吞作用,它涉及形成由网格蛋白三聚体组成的复杂晶格,形成刚毛外观的内体,可通过EM进行形态学鉴定。
无论涉及何种机制,内吞物质都会在细胞内得到加工,包括通过内溶酶体途径的运输。标记降解的物质从早期内体进展到晚期内体,然后进入其在溶酶体中的最终目的地。另外,内吞的物质可以通过回收内吞体重新回到细胞表面。其他运输结果是转胞作用到内腔空间或分选到不同的亚细胞区室,如高尔基复合体和内质网。细胞内转运率也可能因内吞机制而异。例如,已证实网格蛋白介导的内吞作用存在从早期内体返回细胞表面的快速再循环途径。同样,通过巨胞饮和吞噬作用内化的内容物也可能被回收,但更典型的是被加工用于溶酶体降解。有趣的是,在内皮细胞中,通过小窝介导的内吞作用内化的配体优先分选到亚细胞区室中,以避免溶酶体降解途径。
总体而言,上述宏观和微观内吞过程均可能有助于ADC被摄取进入正常细胞。关于正常细胞对ADC的非靶点依赖性摄取相关毒性,小窝依赖性内吞、巨胞饮和吞噬作用等非特异性内吞机制是潜在的重要机制。很明显,不同正常组织和细胞类型的内吞机制和内吞总体速率也不同。许多特殊的免疫细胞(包括巨噬细胞和树突状细胞)特异性地将此作为主要功能,并且具有更高的内吞率。例如,已知Kupffer细胞(肝脏中的固有巨噬细胞)在免疫结合物(包括ADC)的非特异性摄取和清除中发挥着重要作用。内皮细胞由于其在血管与间质室界面的战略定位,大分子的内吞率也相对较高。然而,目前尚未发表关于哪些正常细胞类型和组织在细胞内活性最强的完整描述。因此,了解不同正常细胞/组织中的内吞速率对于理解非特异性内吞作为ADC摄取和毒性的潜在机制的作用具有重要价值。
2.1 影响IgG/ADC非特异性内吞作用的因素大分子的理化性质可能影响其在正常细胞/组织中被内吞的可能性。IgG/ADC表面的分子电荷是共同影响抗体组织分布和PK的许多参数中的一个重要参数。带正电荷的分子被大多数哺乳动物细胞膜以及细胞外基质(硫酸肝素蛋白聚糖)中带负电荷的基团吸引,这种近距离的聚集增加了局部浓度,从而导致正常组织/细胞中更多的非特异性内吞摄取。既往调查性研究表明,IgG抗体净正电荷的增加导致血浆清除率增加,组织分布增加,而净正电荷的减少会导致组织分布减少。重要的是,等电点(pI)变化至少1个单位或以上足以产生可测量的组织分布和PK变化。这些结论也可能适用于ADC,支持ADC电荷可能影响正常细胞非特异性内吞作用的假设。因此,在未来的ADC设计方面,通过减少正电荷或平衡整体表面电荷分布来进行电荷修饰是一种值得考虑的方法。但需要注意的是,与正常组织相似,电荷修饰也可能影响肿瘤细胞疗效相关的靶抗原依赖性ADC摄取。优化ADC表面电荷以减少正常细胞的非靶点依赖性摄取,同时保留肿瘤细胞的靶点介导摄取,可有利改善ADC的治疗指数。
ADC的疏水性也可能在其被正常细胞非特异性摄取中发挥作用。ADC中使用的许多药物-连接子组合具有疏水性,尤其是对于具有高DAR的ADC。高DAR ADC疏水性的增加主要通过Kupffer细胞和肝窦内皮细胞促进ADC聚集和加速非特异性清除。与肝细胞相似,具有高DAR的ADC可能被其他具有较高非特异性内吞能力的正常细胞迅速清除,导致非靶点依赖性(脱靶)毒性。例如,对于基于MMAE的ADC,在体内小鼠模型中,DAR=4纯化ADC的耐受性是DAR=8的ADC的2倍[4]。该结论通常也适用于其他ADC,因此DAR优化是改善ADC治疗指数的关键设计参数。偶联和连接子技术的最新进展可能克服高DAR ADC的这些不必要的PK问题。例如,拟通过改造药物连接子的疏水性或使用聚乙二醇(PEG)掩盖其固有的疏水性来降低ADC整体的疏水性,从而降低较高DAR组分的非特异性清除率,以改善ADC的PK特征和治疗指数。
2.2 与非特异性内吞作用相关的ADC毒性非特异性内吞作用(尤其是巨胞饮)被认为是正常角膜上皮细胞和巨核细胞摄取ADC的途径,分别导致眼毒性和血小板减少症。巨噬细胞介导的角膜上皮细胞摄取的证据主要是由于人原代角膜上皮细胞(体外)对AGS-16C3F (靶向ENPP3抗原,含mc-MMAF连接子-有效载荷的ADC)的细胞毒性降低,其正电荷和/或疏水性降低,并且与EIPA [5-(n -乙基- n -异丙基)-amiloride(巨噬细胞抑制剂)]共同抑制ADC摄取[5]。在这项研究中,作者通过3种不同的机制改变了ADC电荷或疏水性,包括添加聚谷氨酸肽的连接子、某些带电氨基酸的突变改变以及PEG基团与抗体的连接。在角膜上皮细胞中的这些实验结果与电荷修饰(增加净正电荷)改变正常细胞中ADC摄取和毒性的假设基本一致。在产生的9种突变抗体ADC(带负电荷的氨基酸数量增加)中,3种在体外人角膜上皮细胞中显示治疗指数改善[5]。
作者进一步报道了电荷修饰工程化ADC(正电荷减少)在其他一些正常细胞类型(HUVEC和成纤维细胞)中的摄取和毒性较低;然而,在巨核细胞中没有观察到一致的改善,先前报道巨核细胞对相同的非特异性摄取机制敏感[2]。此外,很难将本研究中正常角膜上皮细胞的体外结果与实际体内改善相关联,因为使用的兔模型中的眼部结果显示,在角膜上皮细胞中没有任何病变/缺陷(细胞毒性),正如其他ADC在临床或其他动物模型中所报告的。
本研究结果总体上为电荷在人角膜上皮细胞非靶点依赖性摄取中的重要性提供有力证据,但关于摄取机制主要是巨胞饮的结论仍有待确定。ADC电荷修饰也可能影响角膜上皮细胞中其他潜在受体(FcγRs、CLRs)介导的摄取机制,本研究未完全排除这些机制。
同样,调节巨胞饮介导的内化可降低ADC(AGS-16C3F)对巨核细胞的毒性(血小板减少症)。然而,文献中关于巨胞饮作为分化巨核细胞对于ADC的靶点依赖性摄取机制存在一些不一致。通过电子显微镜(EM)评价可最终确定巨胞饮,通过观察到“皱褶”巨胞饮小体形态。EM评价结合标记的ADC有助于进一步证实正常细胞中巨胞饮介导的ADC摄取和亚细胞定位的参与。
未完待续,有关受体介导的摄取机制等相关内容,详情详见深入探讨正常细胞中ADC非靶点依赖性摄取和相关毒性的潜在机制(下篇)。
参考文献:
[1]Mahalingaiah PK, Ciurlionis R, Durbin KR, et al. Potential mechanisms of target-independent uptake and toxicity of antibody-drug conjugates. Pharmacol Ther. 2019 Aug;200:110-125.
[2]Zhao H, Gulesserian S, Ganesan SK, et al. Inhibition of megakaryocyte differentiation by antibody-drug conjugates (ADCs) is mediated by macropinocytosis: Implications for ADC-induced thrombocytopenia. Molecular Cancer Therapeutics 16, 1877–1886.
[3]Tolcher AW, Ochoa L, Hammond LA, et al. Cantuzumab mertansine, a maytansinoid immunoconjugate directed to the CanAg antigen: a phase I, pharmacokinetic, and biologic correlative study. J Clin Oncol. 2003 Jan 15;21(2):211-22.
[4]Hamblett KJ, Senter PD, Chace DF, et al. Effects of drug loading on the antitumor activity of a monoclonal antibody drug conjugate. Clin Cancer Res. 2004 Oct 15;10(20):7063-70.
[5]Zhao H, Atkinson J, Gulesserian S, et al. Modulation of Macropinocytosis-Mediated Internalization Decreases Ocular Toxicity of Antibody-Drug Conjugates. Cancer Res. 2018 Apr 15;78(8):2115-2126.
[6]Uppal H, Doudement E, Mahapatra K, et al. Potential mechanisms for thrombocytopenia development with trastuzumab emtansine (T-DM1). Clin Cancer Res. 2015 Jan 1;21(1):123-33.
[7]Guffroy M, Falahatpisheh H, Biddle K, et al. Liver Microvascular Injury and Thrombocytopenia of Antibody-Calicheamicin Conjugates in Cynomolgus Monkeys-Mechanism and Monitoring. Clin Cancer Res. 2017 Apr 1;23(7):1760-1770.
[8]Hoffmeister KM, Falet H. Platelet clearance by the hepatic Ashwell-Morrell receptor: mechanisms and biological significance. Thromb Res. 2016 May;141 Suppl 2(Suppl 2):S68-72.
材料由阿斯利康支持,仅供医疗卫生专业人士参考
审批编号:CN-116519 过期日期:2024-6-19
* 此文仅用于向医学人士提供科学信息,不代表本平台观点

