#UDI# #DI# #PI#

1.问:医疗器械唯一标识的稳定性是指什么?
答:是指唯一标识一旦分配给医疗器械产品,只要其基本特征没有发生变化,产品标识就应该保持不变。当医疗器械停止销售、使用时,其产品标识不得用于其他医疗器械;重新销售、使用时,可使用原产品标识。(《医疗器械唯一标识系统规则》解读)
2.问:医疗器械唯一标识的可扩展性是指什么?
答:是指唯一标识应当与监管要求和实际应用不断发展相适应,“唯一”一词并不意味着对单个产品进行序列号化管理,在唯一标识中,生产标识可以和产品标识联合使用,实现规格型号、批次和单个产品三个层次的唯一性,从而满足当前和未来对医疗器械的识别需求。(《医疗器械唯一标识系统规则》解读)
3.问:发码机构需要具备什么样的资质,其职责和义务有哪些?
答:器械唯一标识的发码机构应当为中国境内的法人机构,具备完善的管理制度和运行体系,确保按照其标准创建的医疗器械唯一标识的唯一性,并符合我国数据安全有关要求。
发码机构应当向注册人/备案人提供执行其标准的流程并指导实施,为便于注册人/备案人等掌握发码机构的编码标准,供相关方选择或应用,发码机构应当将其编码标准上传至医疗器械唯一标识数据库并动态维护。每年 1 月 31 日前,发码机构应当向国家药品监督管理局提交按照其标准创建的唯一标识上一年度的报告。(《医疗器械唯一标识系统规则》解读)
4. 问:目前符合要求的发码机构有哪几家?
答:分别是“中国物品编码中心”、“中关村工信二维码技术研究院”和“阿里健康科技(中国)有限公司”。

5.问:三家发码机构对应的码制是什么?
答:“中国物品编码中心”发行的代码为 GS1 码;“中关村工信二维码技术研究院”发行的代码为 MA 码;“阿里健康科技(中国)有限公司”发行的代码为 AHM 码。
6.问:GS1 码是由哪些信息组成的?
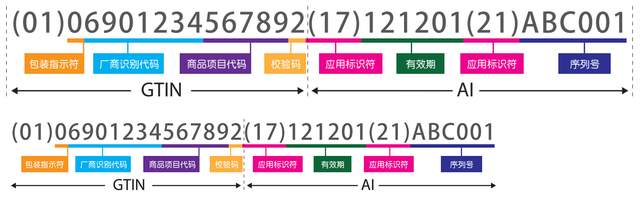
DI:厂商识别代码由 7~10 位数字组成,中国物品编码中心负责分配和管理。厂商识别代码的前 3 位代码为前缀码,国际物品编码协会已分配给中国物品编码中心的前缀码为690~699;商品项目代码由厂商识别代码所有人(即商品条码系统成员)依据有关国家标准自行分配;校验码由标准算法得出。
PI:包含医疗器械序列号、生产批号、生产日期、失效日期等。(基于 GS1 标准的唯一器械标识(UDI)编制规范实现医疗器械可追溯-中国物品编码中心)
7.问:MA 码是由哪些信息组成的?

答:DI:由国家前缀码 3 位;行业标识符 2 位;注册人代码6 位;包装指示符 1 位;产品代码 6 位;校验码 1 位组成。
PI:包含医疗器械序列号、生产批号、生产日期、失效日期等。(UDI 发码服务平台- idcode.org.cn))
8. 问:AHM 码是由哪些信息组成的?

答:第一单元部分为产品资源码:追溯码前 7 位,包含企业信息、药品名称、剂型、批准文号、包装规格等信息,方便产品识别;第二单元部分为单件序列:追溯码 8 到 16 位,是单件商品序列号;最后单元部分为校验位:追溯码 17 到20 位,校验位由特殊加密算法生成。(“码上放心”追溯平台药品追溯码编码规范)
9.问:UDI 数据载体有哪些形式和要求?
答:医疗器械唯一标识数据载体应当满足自动识别和数据采集技术以及人工识读的要求。自动识别和数据采集技术包括一维码、二维码或者射频标签等形式。采用一维码时,可将产品标识和生产标识串联,也可多行并联;采用射频标签时,应当同时具备一维码或者二维码。(《医疗器械唯一标识系统规则》第十一条)
10. 问:如何选择医疗器械唯一标识数据载体?
答:一维码是只在一维方向上表示信息的条码符号,应用多年已经很成熟,成本低,能很好兼容市面上现有的扫码设备,但一维码所占空间大,破损纠错能力差。
二维码是在二维方向上都表示信息的条码符号,相比于一维码,相同空间能够容纳更多的数据,在器械包装尺寸受限的时候能发挥很好的作用,具备一定的纠错能力,但对识读设备的要求相较于一维码要高。
射频标签具有信息存储功能,能接收读写器的电磁调制信号,并返回相应信号的数据载体。射频标签的载体成本和识读设备成本相较于一维码和二维码要高,但 RFID 读取速度快,可以实现批量读取,在某些环节和领域能够发挥作用。
注册人/备案人可根据产品的特征、价值、主要应用场景等因素选择适当的医疗器械唯一标识数据载体。(《医疗器械唯一标识系统规则》解读)
