创新药出海是一场时间和质量的竞赛,中国创新药企需要做好内需与出海的策略平衡,更好实现差异化产品与国际化运营。
政策支持与市场需求共振,加速了我国创新药企的全球化拓展进程。经历资金、技术、法规和市场适应性上的多重考验,以技术突围,以灵活“身段”获利的中国创新药企逐渐在全球化的牌桌上坐稳席位。并且,面对地缘因素的不确定性、严格的监管与准入壁垒,以及趋紧的融资环境,中国创新药企为其他产业领域想要出海的中国企业做了足够精彩的示范。
出海成绩与亮点特色
全球创新药产业的生态构建已有数十年时间,中国创新药形成初具规模的完整产业形态不过10年时间。但经过多年的积淀,中国创新药企步入爆发期,在业界的定位实现“跟随者”-“并行者”-“领跑者”(部分领域)的转变。目前全球生物医药创新力量的分布情况是,40%在美国,30%在中国,其余份额归为欧洲和日本。

从“跟随者”的角色到站在生物医药科研浪潮的前沿,是三十多年来中国企业在技术研发、市场布局、资本运作等多个层面能力提升的表现,中国创新药已成为全球医药行业中的重要力量。
2023年至今的出海成绩宣告了中国创新药企已深度嵌入全球生物医药产业链的生态位。
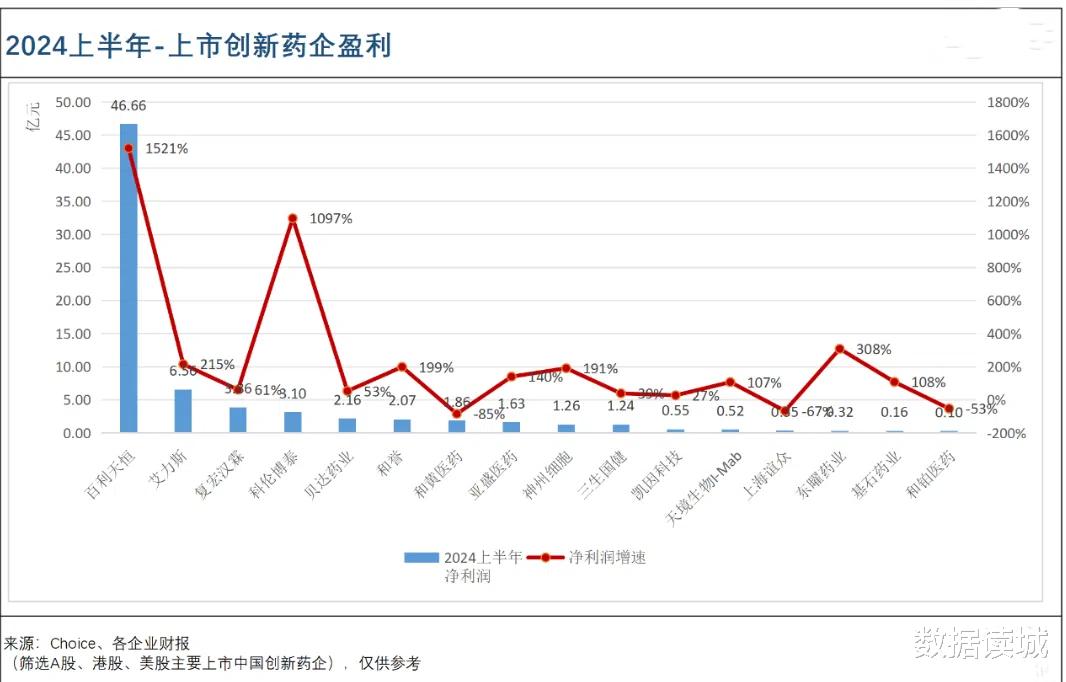
2023年,我国创新药出海交易达69笔,披露总金额超过300亿美元,百利天恒的双抗ADC药物BL-B01D1创下84亿美元的最高单笔授权记录。
2024年,我国创新药出海的交易数量增加、交易总金额双双提高,平均交易首付款有所上升,交易方向进一步拓展,交易模式更为多元化,拿下了更多在国际市场上的发展锚点。当年交易数量达98笔,披露总交易金额接近600亿美元,恒瑞拿下60.35亿美元的年度最高单笔披露金额。同年,我国原研新海外获批13个,超过过往5年获批总和。也是在2024年,我国药品的出海授权数量首次超过从海外引进的数量。
2025年一季度,我国创新药领域的国际授权合作事件已接近2023年全年水平,并超过2024年上半年的交易总额。
创新药企在国内医药市场面临医保控费和同质化竞争的双重压力,而把目标扩展至海外市场顿感“天高地阔”,欧美市场药价基本为中国市场的10-30倍,临床数据获得FDA/EMA等国际权威机构的认可的中国创新药大有可为。从ADC到RNA,从GLP-1到TCE,中国创新药企总能精准地捕捉到国际市场的迫切需求。
政策、资本大力支持
政策与资金的大力支持为创新药出海提供了坚实的保障。
“十四五”以来,我国已有113个国产创新药获批上市,市场规模超千亿元。期间,一系列支持创新药研发的政策起到了很好的助力作用。

政策红利不断的同时,生物医药产业成为新能源和芯片之外最“吸金”的领域,作为技研代表的创新药更是迎来海量资金加持。数据显示,2015年-2024年,创新药企十年来共从一、二级市场筹集到1.23万亿元资金,万亿量级的资本涌入让头部药企有足够的底气围绕创新药推动研发计划并进行市场拓展,上市医药公司也从鲜少涉足创新药到普遍投身所在领域的创新药项目。
最直观的表现便是,我国药企在全球临床研发中的参与度持续提高。从研发管线来看,我国目前的在研创新药管线数量位居全球第二(4804个),仅次于美国(5268个),遥遥领先于英国、韩国、日本等医药产业强国。
竞争环境与模式探索
生物医药产业的国际竞争环境更趋复杂。一方面,不同国家和地区的药品监管体系各不相同,比如美国的FDA、欧盟的EMA、日本的PMDA等,均有着严格的审批流程和要求,侧重点各有不同,中国创新药企需要适应海外监管环境;另一方面,跨国药企主导国际市场多年,在重点市场设下重重壁垒,中国创新药企想要进入需要厘清竞合关系,自行搭建市场准入、定价、销售网络等体系效率不高、风险过大,缺乏海外市场独立运营经验的中国创新药企需要认真选择拓展合作模式及合作对象。
根据市场情况与产品优势,当前中国创新药企主要通过自主研发、License-out(授权出海)、NewCo模式和CSO合作等方式加速融入全球创新体系。
波士顿咨询的分析报告显示,2022年至2024年,全球TOP20的跨国药企中有13家与中国创新药企达成42项BD交易,总交易金额达到593亿美元。中国创新药企的产品在国际市场上认可度持续提升,首付款与里程碑付款金额均呈现提升趋势,利好企业选择BD模式进行出海开拓。
另一个被广泛采用的NewCo模式,是指资本组局成立NewCo,药企将管线剥离给NewCo,获得授权费用及股权。2024年至今,众多头部药企通过NewCo模式实现出海,对于药企而言,这是阶段性解决产品研发向前推动的上佳选择。新药研发过程漫长、复杂且多元,与传统的License-Out模式相比,采用NewCo模式的中国药企能够保留部分股权,既获得授权和里程碑收入,也能在后续新公司价值提升中获益,实现“借助资本力量,加速海外市场布局,提高产品全球竞争力”的目标。
在出海难度最高的创新药领域,从License-out到NewCo模式,中国药企以灵活“身段”与自主性更强的策略避免被资本深度控制,且获得应有的市场席位。
工程创新,输出内卷
科技型产业有着这样的铁律,“技术决定上限,市场与效率决定下限。”
中国企业惯有的效率优势、成本优势在生物医药产业进一步展现。业界普遍认同,开发同样的药物,做到同样的技术标准,中国创新药企所需的成本只有美国同行的二分之一或三分之一。毫不夸张地说,中国创新药企从靶点确认到临床前候选药物的平均时间仅为全球行业平均水平的一半,而人均临床研究成本仅为全球大型制药企业的30%至50%。这也使得一些欧美企业认为不值得研发的细分品类,中国创新药企有更多的机会拿下。

擅长“工程化创新”是中国创新药企的又一特点,同时也是中国创新药出海从“拼产能”到“拼技术”转型的关键。与韩国的优势在于生物药生产端、印度的优势在于仿制药端口相比,我国在仿制药的价格和成本竞争力等方面并不具备明显优势,反倒是持续多年的政策和资本支持,叠加工程师红利,让创新药成为更具潜力的出海方向,这一转变也决定了中国医药产业的未来发展趋势。
中国创新药在发展的初期阶段,多采用“快速跟进”策略,凭借敏锐的市场意识和高效的执行力,快速跟进全球适应症、靶点和技术平台创新进展,利用“中国速度”实现接近同频甚至进度超越。这一阶段面向国内市场居多,我国病人基数大、临床资源丰富的特点,为创新药的发展提供了良好基础,所欠缺的是迅速转化为候选药物的能力。
从无到有的创新,中国创新药企确实不够擅长,但这并不妨碍提升其核心竞争力。某种程度上,这和中国制造在不少领域的全球产业链中所处的生态位一致:基于完善基础设施和工程师红利,擅长工程创新,没有发明新范式或发现新技术,但在现有技术的基础上进行大量优化,通过价格革新确立优势。
业界专家已经提出,在凭借较高的生产研发效率成为“工程化创新”的典范后,中国创新药企接下来的要做的就是如何把产业化的效率提升到国际水平。备受海外医药巨头和资本追捧的中国创新药企,是时候在基础性技术方面,如mRNA、基因编辑、双抗等深研,不客气的说法是,“不能总是美国企业率先取得突破,中国公司再来跟进,美国企业完成从0到1,中国公司完成从1到10、从1到100”。
好在全球市场对中国创新药的认知已经在改变。全球创新药共涉及1840个靶点,其中中国原研创新药覆盖了754个靶点。在Top20热门靶点上,中国与全球的重合度达到80%,且中国在全球热门靶点中的贡献度最高,Top20靶点中有18个靶点的药品数量在全球占比超过50%。2024年美国批准的新药研究申请(IND)的分子中,超过50%的分子来自中国,中国生物医药产业有望迎来自己的DeepSeek时刻。
关税政策暂影响较浅
“能出海就早点出海”是目前中国创新药企的新常态。
不断升级的关税战对我国生物医药产业发展造成影响,攀升的关税已经让仿制药供应链发生变化,即便大多数化学药和生物药的进口关税明确被豁免,尤其是创新药被明确豁免,中国药企对美出口的利润空间仍存在较多的不确定性,全球原料药价格产生波动。目前的具体情况是,部分美国产药品面临关税冲击,中国创新药企所受影响并不大。
在关税战升级之前,美国国立卫生研究院(NIH)已经禁止我国机构访问NIH受控访问数据存储库,这对中国生物医药企业及机构的研发所造成的不利影响程度不一。对此,中国从业者需要明确的是,生物医药是典型的高精尖产业,“产品不是重点,人才、资金、数据和信息流才是。

与其他领域有所差别,生物医药产业高度全球分工合作,全球范围的医药创新需要各方的合作共赢,区域保护主义的旗帜并不是特别好使。面对美国通过关税、监管等手段想要拿捏生物医药产业链主导权,中美科技脱钩风险加剧的局面,中国创新药企一直探行的本地化生产、多元化市场布局和技术合作等方法,都需要根据实际情况做出调整,比如加大对欧洲、东南亚、非洲及拉美等市场的投入。但因有高价值特性,不少中国创新药企仍冀望以高价值创新药精准切入美国市场。
有观点提出,日本药企的全球化发展范例可供我国创新药企借鉴,比如从Me-better(优化改良型)产品切入国际市场、与跨国药企共同开发新产品、在全球范围内布局研发、市场和生产体系等,但中国创新药企所面对的竞争激烈程度,以及全球地缘因素,远比当年的日本药企更显复杂。即便有AI技术和大数据的支持,研发效率大为提高,中国创新药企想要踏实构建全球化的研发中心和本土化管理团队,需要考虑地更深远,解决更多的隐患问题,当前的关税战就需要中国创新药企认真识变应变,因“变”施策。
