2024年9月7日,商务部、国家药监局、国家卫健委三部联合发文《关于在医疗领域开展扩大开放试点工作的通知》,文中提到:在北京、上海、广东、海南等自贸区,允许外资企业从事人体干细胞技术开发和应用。这一政策的出台仿佛一股强劲的东风,为中国干细胞治疗行业注入新的活力,预示着一个机遇无限的黄金时代正在开启。

干细胞治疗是未来的趋势
干细胞作为一种“活”的细胞药物,必须确保进入临床的每一剂细胞质量都是可靠的,而保障干细胞药物安全性的第一关便是培养基。干细胞培养基沿袭几十年抗体药生产的CHO培养基、293培养基的发展历程,也经历了从血清形式、血替形式,到无血清形式。因其无人源、无动物源、成分明确等特点,消除了很多致敏、致病以及未知的风险隐患,越来越多的被更多药企所青睐。
中国首个干细胞培养基FDA 510(K)二类证
近日,友康生物的间充质干细胞无血清培养套装在美国FDA的510(K)二类医疗器械注册获得批准,510(K)号K232543,是美国FDA发放的全球第2个,中国首个该产品的注册证。

产品货号:NC0103+NC0103.S
FDA 510(K)即上市前通告,旨在证明所申请上市的产品和已在美国市场上合法销售的产品在安全性和有效性方面比较是实质等同性相等的(Substantially Equivalent)。这一引入市场的新产品的特性不会对安全性或有效性产生影响,或者对安全有效性产生影响的新特性有可接收的科学方法用于评估新技术的影响。FDA对510(K)申请的严格审核,能够确保进入美国市场培养基产品符合一定程度的安全和质量标准,大幅降低了用户评审间充质干细胞培养基的安全性难度,有力保障了下游细胞制品的安全性和有效性。

严格的检测标准验证产品实力
无血清培养基培养后的间充质干细胞,或其分泌的外泌体,经医药企业研发后,将以局部注射或静脉回输形式进入人体,治疗诸如糖尿病等慢性疾病,所以干细胞药物在人体的使用会是持续性的长期性的。
因此,美国食品药品监管部门对该类产品的安全性极为看重,对培养该细胞药物的无血清培养基制定了极为严格的检测标准,并要求申报企业在遍布全球的美国FDA认可的三方检测实验室完成检测工作。
友康在向美国FDA提交间充质干细胞无血清培养基的510(K)申请期间,递交了包括可沥滤物研究、急性全身毒性研究、白兔皮内反应性试验、皮肤致敏研究、白兔热原试验、体外细胞毒性试验、无菌试验等几十项干细胞培养基相关检测报告。这些报告均是由美国FDA认可的国际权威三方检测机构出具,友康的间充质干细胞无血清培养基均通过了以上技术检测。
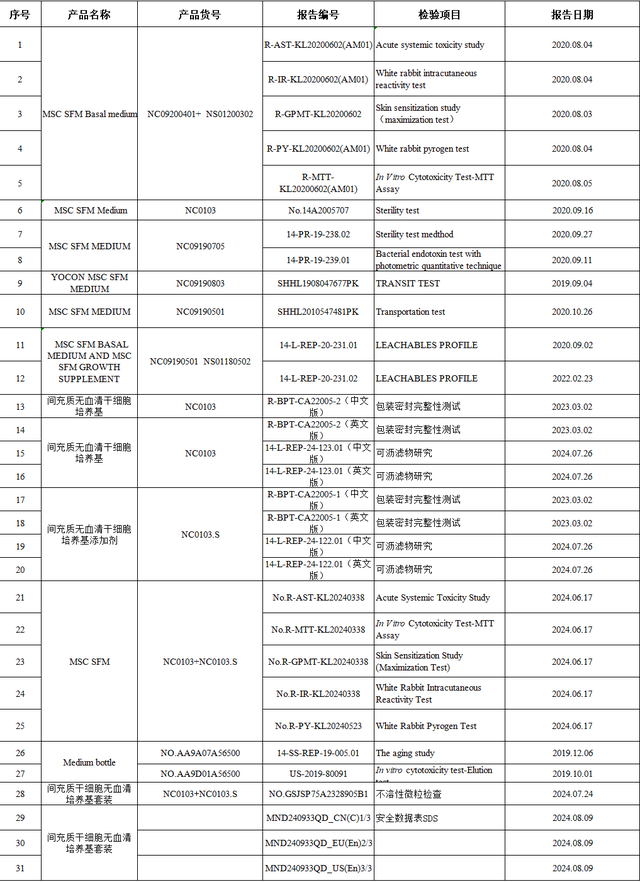


部分检测报告(需要查阅原图加文章里微信)
友康生物2018年在中国市场上推出该产品,并同步启动该产品在美国市场的注册工作。该产品深耕国内多年,已经在国内外拥有上千家客户,助力十余家干细胞药物开发企业进行药物申报,并进入不同的临床实验阶段。
该医疗器械二类注册证书的获得,将大大减少中国干细胞药物开发企业在中国市场与美国市场申请干细胞药物的工作量和不确定性,相信能够助力更多药物开发企业早日获得干细胞药物销售的市场准入。
关于友康生物友康生物成立于2006年,产品聚焦无血清细胞培养与分子检测。历经18年发展,公司已经形成种类比较齐全的产品体系。无血清细胞培养方面,形成了干细胞、免疫细胞、工程细胞、辅助生殖四大产品体系。分子检测方面,形成了样本采集、核酸快速提取、支原体细菌真菌检测三大产品体系。产品形式从公司成立之初的单一试剂的手工使用产品,扩展到了现在的集成试剂、高分子材料、自动化设备的自动化产品。实现了“从墨水到打印机”的产品升级。

为满足越来越多的中国药企出海的要求,友康生物2021年在北京投资建设的新研发生产基地已于2024年5月份正式启用。该基地投资2.5亿,按照能够同时满足中国药监局、美国FDA的监管要求建设。所有生产设备全部选用可同时通过中国药监局与美国FDA双认证的国内顶尖制药设备企业产品,无菌产品B+A的生产环境,与客户细胞药物生产环境要求完全一致。能够完美支持更多客户在中国与美国同时进行药物申报与药物生产的硬件要求。

— END —

- 科普 情怀 责任 -
