
免疫治疗打破BTC十年沉寂僵局。
胆道系统恶性肿瘤(BTC)占所有消化道恶性肿瘤3%[1],由于早期缺乏特异性症状,侵袭性极高,绝大多数患者就诊时已为晚期,失去手术机会,预后极差。十余年来,吉西他滨联合顺铂(GC)方案带来的生存获益有限,中位总生存期(mOS)不足1年[2],亟待更有效的诊疗方案。近年来,免疫检查点抑制剂(ICI)如火如荼发展,改变了多个恶性肿瘤诊疗格局,在BTC领域也在进行探索性尝试,然而多数免疫治疗相关研究在Ⅱ期阶段就已沉沙折戟,治疗进展停滞不前。直至2022年美国临床肿瘤学会消化道肿瘤研讨会(ASCO GI)上正式公布了全球首个BTC一线治疗获得阳性结果的Ⅲ期TOPAZ-1研究,标志着BTC领域正式迎来免疫治疗新时代。展露锋芒,TOPAZ-1研究建立标准治疗3.0ABC02研究[3]提示GC方案较吉西他滨单药化疗一线治疗BTC显著提升OS和无进展生存期(PFS),建立了GC双药化疗在晚期BTC的一线标准治疗方案,但数十年来难以有新突破。随着对免疫治疗机制的探索和研究的深入,免疫治疗在肺癌、黑色素瘤、食管癌等多个恶性肿瘤领域获批适应症。在BTC领域中,免疫治疗也成为了晚期BTC治疗的研究热点,其中针对PD-1/PD-L1通路的ICIs备受关注,也表现出了良好的治疗潜力。研究显示化疗可以上调BTC中PD-L1表达并改变免疫细胞浸润[4],提示免疫联合化疗或可为BTC治疗带来生存获益可能。从治疗机制上看,免疫联合化疗也已被多次被证实具有协同增效作用。TOPAZ-1研究是目前*首个且唯一在BTC一线治疗领域获得成功的Ⅲ期临床研究,OS、PFS和客观缓解率(ORR)均获得有统计学意义的阳性结果。基于TOPAZ-1研究的惊艳结果,度伐利尤单抗单抗+化疗方案纳入《CSCO胆道恶性肿瘤诊疗2022》一线治疗Ⅰ级推荐(ⅠA类证据),BTC一线治疗从单药化疗到GC双药化疗,进入标准治疗3.0时代。三阳开泰,首个BTC领域OS/PFS/ORR均获益的Ⅲ期研究TOPAZ-1研究[5]设计:共入组了685例局晚期、复发性或转移性BTC患者,包括肝内和肝外胆管癌和胆囊癌(排除壶腹癌)。在17个国家的145个中心进行,其中55%的患者来自亚洲。研究主要终点是OS,次要终点包括PFS、ORR和安全性。685名患者被随机分为度伐利尤单抗+GC化疗组(n=341)或安慰剂+GC化疗组(n=344)。

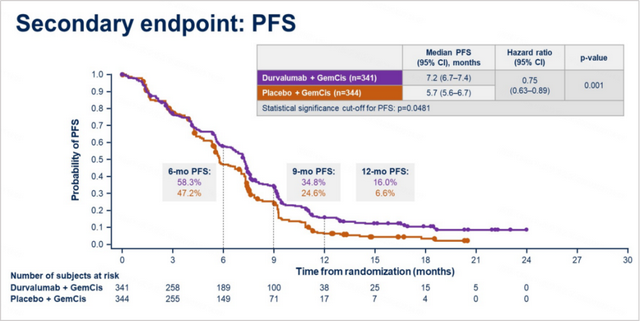
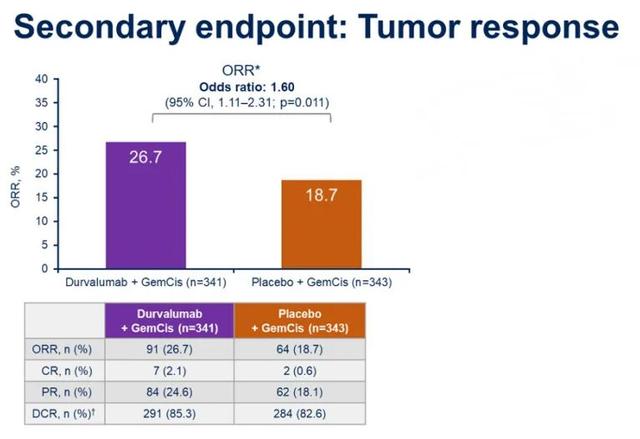 图4 ORR(来源2022 ASCO GI)亚洲人群OS达13.6个月,
图4 ORR(来源2022 ASCO GI)亚洲人群OS达13.6个月,ESMO更新OS夯实一线标准
上述ESMO更新的OS数据证实了度伐利尤单抗+化疗方案为晚期BTC患者带来了生存获益,夯实了一线治疗标准。在2022 ASCO上,研究公布了不同地区的亚组数据[7],其中亚洲人群OS达到13.6个月,度伐利尤单抗+化疗组较安慰剂+化疗组延长了2个月OS,降低死亡风险接近30%(HR=0.72,95%CI:0.56-0.93)。从PFS数据观察,疾病进展或死亡风险同步下降,在接受度伐利尤单抗+化疗治疗后,亚洲人群的疾病进展或死亡风险下降33%(vs全球人群25%)。免疫联合化疗在不同地域间、不同人种间均能降低疾病进展或死亡风险,且在亚洲人群上获益更加明显。


TOPAZ-1研究的成功无疑是BTC领域免疫治疗的里程碑,一举将晚期BTC带入免疫治疗时代。2022 ESMO更新的OS数据进一步夯实了度伐利尤单抗联合化疗的BTC一线治疗标准,且在亚洲人群中获益更为显著。在两大商业保险、三大阳性结果和四大权威指南的助力和护航下,期待在度伐利尤单抗标准治疗3.0基础上能有更多联合治疗方案的进一步探索,为更多BTC患者带来更多生存获益可能。
*截至发稿日止参考文献:[1]BRAY F,FERLAY J,SOERJOMATARAM I,et al.Global cancer statistics 2018:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J].CA Cancer J Clin,2018,68:394-424.[2].宗源,周军,沈琳.晚期胆管癌的药物治疗现状[J].中华临床医师杂志(电子版),2019,13(3):214-220.[3]Valle J,Wasan H,Palmer DH,et al.Cisplatin plus gemcitabine versus gemcitabine for biliary tract cancer.N Engl J Med 2010,362(14):1273-1281.[4]Koido S,Kan S,Yoshida K,et al.Immunogenic modulation of cholangiocarcinoma cells by chemoimmunotherapy.Anticancer Res.2014 Nov;34(11):6353-61.[5]Do-Youn Oh,MD,ph D,et al.A phase 3 randomized,double-blind,placebo-controlled study of durvalumab in combination with gemcitabine plus cisplatin(GemCis)in patients(pts)with advanced biliary tract cancer(BTC):TOPAZ-1.2022ASCO GI#378[6]Do-Youn Oh,et al.Updated overall survival(OS)from the phase III TOPAZ-1 study of durvalumab(D)or placebo(PBO)plus gemcitabine and cisplatin(+GC)in patients(pts)with advanced biliary tract cancer(BTC).ESMO Asia Congress 2022.Annals of Oncology(2022)33(suppl_9):S1454-S1484.[7]Arndt Vogel,et al.Regional subgroup analysis of the phase 3 TOPAZ-1 study of durvalumab(D)plus gemcitabine and cisplatin(GC)in advanced biliary tract cancer(BTC).2022 ASCO.Journal of Clinical Oncology 2022 40:16_suppl,4075-4075.*医学界力求其发表内容专业、可靠,但不对内容的准确性做出承诺;请相关各方在采用或以此作为决策依据时另行核查。

