5月24日,据NMPA官网正式公告,康方生物的依沃西单抗(AK112/Ivonescimab)已获准在国内上市。这款新药将成为全球首款融合“肿瘤免疫+抗血管”双重机制的双特异性抗体药物,其治疗范畴主要涵盖那些经过EGFR酪氨酸激酶抑制剂(EGFR-TKI)治疗后病情进展的、携带有EGFR突变的局部晚期或转移性非鳞非小细胞肺癌(NSCLC)患者。该品种的上市为NSCLC患者提供了新的治疗选择。

截图来源:NMPA官网
依沃西是康方生物独立自主研发的全球首创PD-1/VEGF双特异性抗体新药,基于本公司独特的Tetrabody技术设计,可阻断PD-1与PD-L1和PD-L2的结合,并同时阻断VEGF与VEGF受体的结合。PD-1抗体与VEGF阻断剂的联合疗法已在多种瘤种(非小细胞肺癌、肾细胞癌和肝细胞癌)中显示出强大的疗效。鉴于VEGF和PD-1在肿瘤微环境中的共表达,与联合疗法相比AK112作为单一药物同时阻断这两个靶点,可能会更有效地阻断这两个通路,从而增强抗肿瘤活性。

截图来源:药融云全球药物研发数据库
2022年12月,依沃西以总交易额高达50亿美金(5亿美金首付款),外加销售净额两位数提成的合作方案,授予美国Summit Therapeutics公司在美国、欧洲、加拿大和日本的开发独家许可权,创下中国单个创新药物对外权益许可最高交易金额纪录。此前,依沃西在肺癌领域的3项适应症已分别获得CDE授予的突破性治疗药物认定。2023年8月,依沃西首个新药上市许可申请(NDA)获得受理,并获优先审评资格。
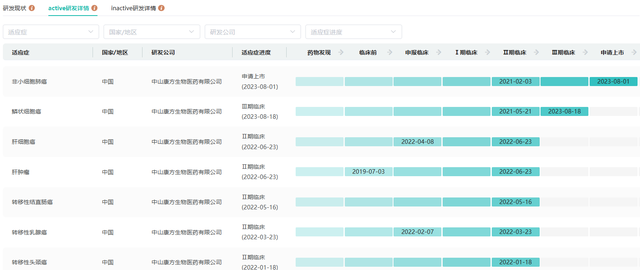
截图来源:药融云全球药物研发数据库
在2022年和2024年ASCO年会上,康方生物公布了关于AK112的临床试验结果。2022年的II期临床试验显示,AK112联合化疗治疗EGFR-TKI失败的EGFR突变晚期非鳞状NSCLC患者,ORR达68.4%,DCR为94.7%,中位PFS为8.2个月。
而2024年的III期临床HARMONi研究显示,中位随访7.89个月后,AK112+化疗组患者的mPFS为7.06个月,明显优于安慰剂+化疗组的4.80个月(HR=0.46,P<0.0001)。亚组分析亦显示AK112在三代EGFR-TKI治疗、脑转移及T790M突变患者中有显著疗效。AK112组ORR为50.6%,高于安慰剂组的35.4%。在策略上,AK112专注于肺癌治疗,旨在解决现有药物难以应对的病种,并抢占大适应症市场,如PD-L+的NSCLC等。
参考来源:
[1] NMPA官网
[2] 药融云数据库
