
编者按:北京大学肿瘤医院沈琳教授团队在国际顶级期刊《Trends in Cancer》(即时IF:17.3)发表题为“Targeting novel immune checkpoints in the B7-H family: advancing cancer immunotherapy from bench to bedside”的综述论文。该研究系统阐述了B7-H家族分子在肿瘤免疫微环境(TME)中的调控机制,并总结了针对该家族成员的临床转化进展,为突破现有免疫治疗瓶颈提供了新方向。

本文第一作者为2021级八年制罗一鸣、2023级博士生袁野、刘丹副主任医师,通讯作者为陈杨副教授和沈琳教授。
通讯作者

沈琳
▶ 北京大学肿瘤医院消化肿瘤内科主任、1期临床试验病区主任
▶ 北京学者、国家重点研发计划首席科学家
▶ 牵头国际国内多项临床研究,促进新药获批适应症13项,研究成果改变国内外临床实践指南30多项。
▶ 以第一/通讯作者,在Nature,BMJ,Nature Medicine,Lancet Oncology, JCO等国际权威期刊发表SCI论文370余篇,他引总计23140次,H指数70。写64部国际国内诊疗规范,获国家专利15项。
▶ 入选全球高被引科学家、全球前2%顶尖科学家、北京市突出贡献专家等:获中华医学科技奖一等奖、中国抗癌协会科技奖一等奖等多项奖项。主要研究方向是消化道肿瘤精准治疗与转化研究、抗肿瘤新药临床研究
研究团队探讨了B7-H免疫检查点家族在癌症免疫治疗中的应用,重点关注B7-H家族成员在TME中的作用及其临床转化潜力。B7-H家族包括B7-H2(ICOSL)、B7-H3、B7-H4、B7-H5(VISTA)、B7-H6和B7-H7(HHLA2)等分子,这些分子在肿瘤免疫调控中起着关键作用。研究显示,B7-H3、B7-H4和VISTA主要发挥免疫抑制作用,而B7-H2和B7-H6则具有协同刺激作用,HHLA2(B7-H7)则表现出双重免疫功能。

(图1.B7H家族成员总览)
B7H2(ICOSL)
ICOSL是一种刺激性免疫检查点分子,主要通过与ICOS受体结合,发挥免疫激活作用,促进T细胞的增殖和细胞因子的分泌,增强抗肿瘤免疫反应。ICOSL的激活能够有效增强免疫反应,尤其在与其他免疫治疗靶点(如PD-1)联合应用时,展现出明显的协同效应。
B7H3(CD276)
B7-H3是一种抑制性免疫检查点分子,广泛表达于多种肿瘤类型。B7-H3通过抑制CD8+T细胞的活化和增殖,发挥免疫抑制作用,但其受体目前仍不明确。B7-H3高表达与肿瘤的恶性进展、转移以及患者的预后不良密切相关。目前靶向B7-H3免疫治疗临床研究取得了重要进展。最为显著的是B7-H3的抗体药物偶联物(ADC)疗法与CAR-T细胞治疗,在以肺癌为代表的肿瘤患者中显示出显著的疗效。

(图2. B7-H2和B7-H3在肿瘤免疫微环境中的促肿瘤/抗肿瘤效应以及免疫学作用)
B7H4(B7x,B7S1)
B7-H4是一种抑制性免疫检查点分子,主要通过与T细胞上的未知受体结合,抑制T细胞的激活与功能。B7-H4在多种肿瘤微环境中的高表达,与T细胞功能的衰竭、免疫逃逸以及肿瘤的耐药性密切相关。其表达水平在多种癌症中均显著上调,如卵巢癌、肾癌、乳腺癌等,并且与不良预后相关。目前靶向B7-H4的ADC药物的临床试验中取得了一定成果。临床试验中,B7-H4的ADC治疗展现了在多种恶性肿瘤中的良好疗效,尤其在乳腺癌、卵巢癌和胆管癌的治疗中。
B7H5(VISTA)
VISTA是一种新型的免疫检查点分子,在肿瘤浸润巨噬细胞中存在显著表达。在酸性肿瘤微环境(pH=6.0)中,VISTA通过与PSGL-1结合,抑制T细胞的活性,促进T细胞衰竭并增强调节性T细胞(Treg)的功能。VISTA的高表达通常与肿瘤的免疫逃逸、耐药性相关,但其展示出矛盾的预后关系。临床前实验表明,抗VISTA治疗能够有效恢复T细胞的功能,抗VISTA疗法显示出与传统PD-1抑制剂联合应用时的协同效应。目前多项靶向VISTA的临床试验正处于1期进行阶段。
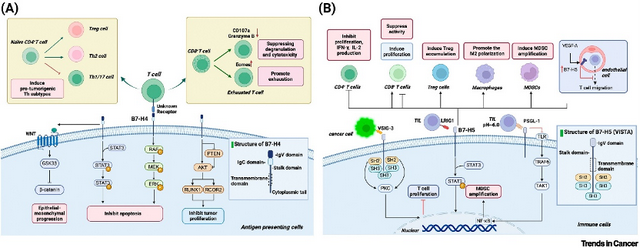
(图3. B7-H4和B7-H5在肿瘤免疫微环境中的促肿瘤/抗肿瘤效应以及免疫学作用)
B7H6
B7-H6是一种刺激性免疫分子,主要通过与NK细胞NKp30受体结合,激活NK细胞免疫反应,从而增强对肿瘤细胞的杀伤作用。但同时B7-H6在肿瘤细胞表面存在显著表达,其通过激活多种下游信号通路促进肿瘤细胞增殖和转移。B7-H6的临床应用处于早期阶段,目前两项靶向CD3/B7-H6的双特异性T细胞衔接器(BiTE)正在1期临床试验阶段。
B7H7(HHLA2)
B7H7(HHLA2)是B7-H家族中的新成员,表现出双重免疫功能,可通过与TMIGD2受体结合增强免疫反应,也能通过与KIR3DL3受体结合抑制免疫反应。在肿瘤微环境中,HHLA2的表达通常较高,并与肿瘤的免疫逃逸及转移能力密切相关。多个靶向HHLA2的早期临床试验正在进行中,值得注意的是,靶向阻断HHLA2-KIR3DL3轴的药物可能具有更高治疗潜力。

(图4.B7-H6和B7-H7在肿瘤免疫微环境中的促肿瘤/抗肿瘤效应以及免疫学作用)
综上所述,B7-H家族成员在肿瘤免疫治疗中扮演着关键角色,涵盖了免疫激活(如ICOSL、B7-H6)和免疫抑制(如B7-H3、B7-H4、VISTA)的分子。随着临床研究的深入,这些靶点为癌症免疫治疗带来了新的突破,推动了从基础到临床的转化应用。
原文链接:Luo Y, Yuan Y, Liu D, Peng H, Shen L, Chen Y. Targeting novel immune checkpoints in the B7-H family: advancing cancer immunotherapy from bench to bedside. Trends Cancer. 2025 Mar 19:S2405-8033(25)00055-X. doi: 10.1016/j.trecan. 2025.02.007. Epub ahead of print. PMID: 40113530.
推荐您看
版权声明
本文版权归“北京大学肿瘤医院消化内科”所有。
