2月16日,Iovance Biotherapeutics公司宣布,FDA加速批准该公司的肿瘤浸润淋巴细胞(TIL)疗法Amtagvi(lifileucel)上市,用于治疗晚期黑色素瘤。据悉,lifileucel是全球首款获批上市的TIL细胞疗法。
Iovance Biotherapeutics公布的资料显示,单剂量的Amtagvi包含7.5亿到72亿个活细胞,从收到肿瘤组织到完成Amtagvi制备大约需要34天,AMTAGVI 将装在 1-4 个患者专用输液袋中,每袋含有 100 mL 至 125 mL 的活细胞。

什么是TIL疗法
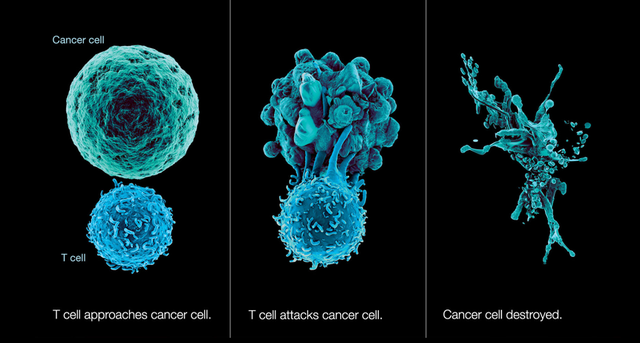
TIL存在于肿瘤组织间质中,是由CD8+T细胞、CD4+T细胞、B细胞、NK细胞与γδT细胞等组成的异质性细胞群体,其中对肿瘤细胞的直接杀伤性主要通过细胞毒性CD8+T细胞来实现。然而,由于肿瘤组织中免疫抑制微环境的存在,往往会导致肿瘤组织中的TIL的扩增及抗肿瘤活性被抑制。TIL疗法则通过从患者自身肿瘤组织中分离出TIL,体外刺激扩增筛选后,将具有抗肿瘤作用的免疫细胞回输给患者。


Amtagvi(lifileucel)主要疗效
主要疗效分析集包括来自队列4的73名患者,他们从批准的生产工厂接受了推荐剂量的lifileucel。在73例患者中,31.5%的患者根据实体瘤应答评价标准(RECIST 1.1)达到客观缓解,随访18.6个月时中位缓解持续时间未达到(43.5%的缓解持续时间大于12个月)。此外,支持合并疗效集包括来自队列4和队列2的153名患者。153例患者中,31.4%通过RECIST 1.1获得客观缓解,随访21.5个月时中位缓解持续时间未达到(54.2%的缓解持续时间大于12个月)。国内外TIL疗法领域公司盘点
lovance BiotherapeutisIovance Biotherapeutics是TIL细胞疗法领域的领头羊。2019年5月,美国FDA授予Iovance Biotherapeutics公司的LN-145(TIL疗法)突破性疗法认定,用于治疗在接受化疗后复发、转移性或持久性宫颈癌患者。
除了LN-144和LN-145,lovance公司管线中的LN-145-S1(PD-1选择性TIL疗法)、LN-145-Gen 3(第三代TIL疗法)也都已进入到了2期或3期临床试验阶段,涉及头颈鳞状细胞癌(HNSCC)、转移性非小细胞肺癌(NSCLC)等适应症。
刚批准的Amtagvi(lifileucel)就是此公司
Obsidian TherapeuticsObsidian Therapeutics是一家致力于开发工程细胞和基因疗法的医药公司。cytoTIL15是Obsidian的先导cytoTIL项目,目前处于临床前开发阶段,用于治疗转移性黑色素瘤和其他实体瘤。其独特之处是,TIL细胞表达IL-15,不再需要接受IL-2的治疗,在提高TIL疗法持久性的同时降低了疗法的毒副作用。
Instil BioInstil Bio是一家临床阶段生物医药公司,专注于开发TIL疗法治疗癌症。ITIL-168是该公司的同种自体TIL疗法,治疗PD-1抑制剂耐药/复发的晚期黑色素瘤,已处于2期临床试验阶段。此外,ITIL-168还拟被开发用于治疗皮肤鳞状细胞癌(CSCC)、非小细胞肺癌(NSCLC)和宫颈癌等适应症。
卡替医疗卡替医疗是中国TIL/新抗原等创新免疫细胞治疗的代表性企业。ScTIL210是卡替医疗开发的第四代TIL,无需借助手术组织获取TIL细胞,而是从外周血采集单核细胞,分离肿瘤识别性T细胞——从而大大提升了治疗实施的便捷性,并进一步给予基因修饰,提升其克服肿瘤微环境和增加自我扩增的能力。该产品在前期的概念验证临床研究中已取得了非常积极的疗效和安全性。
君塞生物君赛生物是一家致力于开发基于TIL的实体瘤创新疗法的创新企业。目前,公司已建立高效简便的TIL细胞富集培养和高效安全的非病毒载体T细胞基因修饰等核心技术。2021年2月,君赛生物完成近亿元A轮融资,用于推进TIL细胞新药管线的搭建。君赛生物的“自体天然肿瘤浸润淋巴细胞注射液”IND已经获得CDE默示许可,适应症为“成人经标准治疗失败或缺乏有效的治疗方法的、病理诊断明确的不可切除的晚期实体瘤”。
西比曼生物西比曼生物致力于开发治疗癌症的免疫细胞治疗产品和治疗退行性疾病的干细胞治疗产品。产品系列包括针对CD20-、CD22-和B细胞成熟抗原(BCMA)特异性CAR-T化合物的临床前化合物,以及TCR-T细胞技术和TIL细胞技术。
沙砾生物沙砾生物专注于TIL疗法的开发。2021年10月28日,沙砾生物TIL疗法GT101的临床试验申请获得NMPA受理。GT101是一款基于患者自体TIL的细胞药物,通过从患者体内获取肿瘤组织并提取TIL,再经过沙砾生物特有的StemTexpTM生产平台扩增至10亿量级后输注回患者体内以对抗肿瘤。沙砾生物已经完成A+系列融资,用于推进GT101 临床开发。沙砾生物的“GT101注射液”IND已经获得CDE默示许可,适应症为“转移或复发的实体瘤”。
劲风生物劲风生物发展TIL疗法在临床上的应用,治疗治愈实体肿瘤患者,提升患者生命质量。2021年10月宣布完成千万美元的A轮融资,资金将用于公司在2022年初推动其产品管线进入IND阶段以及开展I期临床试验。
原启生物原启生物聚焦于肿瘤免疫治疗领域的新产品开发。公司自主创新建设的OriTIL—细胞高效扩增培养技术平台开发的产品,具有高倍率提升TIL细胞扩增数量和质量属性等特点,可以有效突破TILs疗法的技术瓶颈,确保其临床应用的安全性和有效性。得益于OriTIL的平台优势,原启TILs产品管线已在临床阶段获得了可喜进展,进入临床申报阶段。