一、定义及流行病学
1.定义
在医院外罹患的感染性肺实质炎症包括具有明确潜伏期的病原体感染在入院后于潜伏期内发生的肺炎临床表现不一轻症——发热和咳痰为特征重症——可进展为呼吸窘迫和脓毒症2.流行病学
成人CAP发病率及病死率高,医疗资源耗资巨大
二、危险因素
1.高龄
年龄≥65岁的人群中,CAP的年住院率约2,000/100,000一般人群的3倍,表明每年有2%的老年人因CAP住院2.慢性共病
COPD、支气管扩张、哮喘慢性心脏病(心衰)脑卒中糖尿病营养不良免疫功能缺陷3.病毒性呼吸道感染
流感新冠4.气道保护受损
增加胃内容物大量误吸和/或上呼吸道分泌物微量误吸的风险意识改变(如,脑卒中、癫痫、麻醉、药物或酒精使用所致)吞咽困难(食道病变或动力障碍引起)5.其他
吸烟酗酒使用阿片类药物生活条件(监狱,收容所,油漆、汽油)贫穷三、微生物
(一)微生物类型
1.细菌
肺炎链球菌(最常见)流感嗜血杆菌卡他莫拉菌金黄色葡萄球菌A组链球菌革兰阴性需氧菌肠杆菌科的克雷伯菌属大肠埃希菌微需氧菌和厌氧菌(与误吸有关)2.非典型病原体
军团菌肺炎支原体肺炎衣原体鹦鹉热衣原体3.病毒
甲、乙流COVID-19其他冠状病毒中东呼吸综合征冠状病毒严重急性呼吸综合征冠状病毒等鼻病毒副流感病毒腺病毒呼吸道合胞病毒人类偏肺病毒人博卡病毒(二)微生物影响因素
1.基础疾病

2.病毒感染

(三)病原体的变化趋势
1.肺炎链球菌发病率下降
肺炎球菌疫苗的广泛使用,使得肺炎球菌肺炎个体发生率下降以及群体免疫形成肺炎球菌疫苗接种率有地区差异——肺炎链球菌感染率也有差异欧洲约30%的CAP病例是肺炎链球菌所致,而美国只有10%—15%,而美国的人群肺炎球菌疫苗接种率更高2.COVID-19全球流行
3.mNGS的使用—方法学进步
1/3的成人CAP病例中检测到了呼吸道病毒呼吸道病毒作用尚不确定:作为单一病原体,作为发生细菌性CAP的辅助因素,或触发宿主免疫应答失调。4.病原体总体检出率低
尽管使用分子诊断和其他微生物学检测方法进行广泛评估,仍仅有一半的CAP病例可以确定病原体CAP发病机制的理解还不充分5.肺部微生物群的发现
以前认为肺部是无菌的—非培养技术(即,高通量16SrRNA基因测序)已在肺泡内发现复杂多样的微生物群落这一发现表明,肺泡常驻微生物在肺炎的发生中起一定作用,其机制可能是调节宿主对感染病原体的免疫应答,或肺泡微生物群内特定病原体直接过度生长四、发病机制
1.主要由细菌性或病毒性呼吸道病原体引起
飞沫/气溶胶吸入传播吸入—病原体定植于鼻咽部—微量误吸到达肺泡当接种量足够和/或宿主免疫防御能力受损时,就会发生感染病原体复制、致病因子产生和宿主免疫应答会导致肺实质炎症和损伤,最终引起肺炎2.肺泡微生物群改变(肺泡生态失调)
与常驻微生物竞争才能复制常驻微生物影响或调节宿主对感染病原体的免疫应答3.肺泡内的常驻微生物不受控制的复制
肺泡微生物群与口腔菌群相似主要为厌氧菌[如普氏菌(Prevotella)和韦荣球菌(Veillonella)]以及微需氧性链球菌病毒感染或烟雾暴露等外源性损伤可能改变肺泡微生物群的组成,并触发某些微生物的过度生长由于构成肺泡微生物群的微生物通常不能采用标准培养方法来培养—可能解释了为什么CAP患者中病原体检出率低五、诊断标准
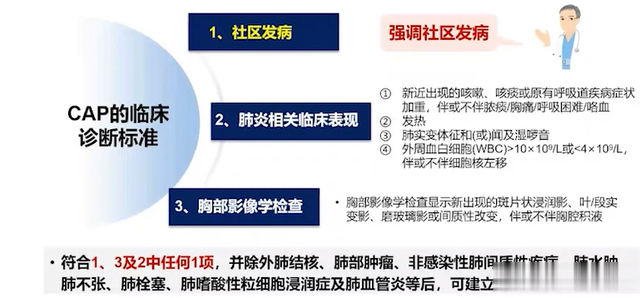
六、病情严重程度评估

1.CURB-65

2.PSI评分

七、病原体推断及经验治疗
1.概述
2016年版《中国成人社区获得性肺炎诊断和治疗指南》提出CAP诊治中的“六步法”:其中核心和难点仍在于推测可能的病原体及其耐药性并及时启动经验性抗感染治疗,因为它关乎初始治疗能否成功,影响疾病预后 CAP诊断过程中最难是对病原体的判断,常需考虑以下问题
CAP诊断过程中最难是对病原体的判断,常需考虑以下问题 2019年ATS/IDSA指南建议:仅重症CAP患者需进行痰培养或血培养因此,轻中度CAP患者的病原学诊断相对更为困难,临床中仅根据患者年龄、基础疾病、临床特点、疾病严重程度、肝肾功能、既往用药等分析最有可能的病原并评估耐药风险
2019年ATS/IDSA指南建议:仅重症CAP患者需进行痰培养或血培养因此,轻中度CAP患者的病原学诊断相对更为困难,临床中仅根据患者年龄、基础疾病、临床特点、疾病严重程度、肝肾功能、既往用药等分析最有可能的病原并评估耐药风险2.我国CAP病原体流行病学的特点
肺炎支原体和肺炎链球菌是我国成人CAP重要病原体其他常见病原体包括流感嗜血杆菌、肺炎衣原体、肺炎克雷伯菌及金黄色葡萄球菌铜绿假单胞菌、鲍曼不动杆菌少见
3.2016年中国CAP指南对病原学检查的推荐意见

4.CAP患者感染病原体耐药问题严峻

5.肺炎耐药评分

6.个体化评估
(1)肺炎链球菌
2009-2010—CARTIPS不敏感肺炎链球菌(PNSP)占10.8%,青霉素耐药肺炎链球菌(PRSP)仅占2%阿奇霉素—一耐药高达88.8%PRSP的危险因素包括过去3个月抗生素暴露、近期住院、两极年龄、接触托儿所儿童等肺炎链球菌一旦对青霉素不敏感:预示着与—内酰胺类抗菌药物发生明显的交叉耐药
(2)金黄色葡萄球菌
新生儿、婴儿:引起新生儿、婴儿重症肺炎的原因之一,表现为呼吸短促、发热,影像学可表现为多发的粗糙的薄壁空洞,易并发气胸和脓胸成人:导致的CAP多发生在先期流感的基础上,患者可出现发热、咳血性痰,表现为坏死性肺炎对于金黄色葡萄球菌,评估其是否对甲氧西林耐药需要审慎CA-MRSA最早20世纪80年代,导致有身体接触的密集人群的皮肤软组织感染(SSTI)2000年左右开始有CA-MRSA导致CAP的报道美国——MRSA-CAP占所有CAP的2.4%,占ICU-CAP的5%中国——针对SSTI的前瞻性队列研究结果显示,在纳入的501例SSTI患者中仅分离出5株CA-MRSA,分离率为3%(5/164)CAP需经验性覆盖MRSA的情况病情危重需要入住ICU、影像学显示坏死或空腔浸润以及出现脓胸如果合格的呼吸道分泌物培养无MRSA生长则停止经验性治疗。我国CAP中MRSA不是常见原因,但仍需高度警惕过去30d内曾使用抗生素治疗过去1年内曾发生MRSA感染或定植肺炎严重程度指数(PSI)评分≥120(3)革兰阴性菌
1)流感嗜血杆菌和卡他莫拉菌
esp:对于吸烟者和慢性阻塞性肺疾病(慢阻肺)患者产生青霉素酶流感嗜血杆菌产酶率15%-20%,而卡他莫拉菌产酶率高达90%常用的头孢菌素、大环内酯以及氟喹诺酮都能有效覆盖2)肺炎克雷伯杆菌
2006年、亚洲、12个国家、CAP的病原体及其敏感性研究显示:肺炎克雷伯杆菌占9.7%,产ESBL者为13%(低于以腹腔感染为出发点的结论)近期抗生素暴露史、高龄、误吸、入住医疗机构以及基础心肺疾病(不包括结构性肺疾病)3)铜绿假单胞菌
感染的风险包括严重结构性肺疾病、重度慢阻肺、近期抗生素暴露史、近期住院特别是入住ICU并接受机械通气(4)非典型病原体
1)支原体
对大环内酯体外耐药比例高体外耐药和临床治疗失败之间的关系研究很少研究表明大环内酯体外耐药可以导致发热时间延长,但并没有影响疾病预后建议在高度怀疑因大环内酯耐药导致治疗失败者改用呼吸喹诺酮类药物治疗2)军团菌
流行病学资料缺乏要高度怀疑军团菌肺炎CAP患者出现发热伴相对缓脉、发作性头痛、非药物性精神神经症状、肺外表现明显诸如非药物性腹泻和急性肝肾损害,实验室检查出现低钠血症特别是低磷血症,以及β内酰胺类抗菌药物治疗无效时军团菌肺炎的影像学表现常为非特异性,可出现多肺叶、多肺段浸润影,出现空洞,部分患者有明显的胸腔积液,且可进展迅速。八、治疗方案
1.两大经典方案比较

2.新型四环素类药物
 抗菌谱广泛,但对铜绿假单胞菌无活性
抗菌谱广泛,但对铜绿假单胞菌无活性 具有良好的安全性优势
具有良好的安全性优势 代谢稳定,药物间相互作用少
代谢稳定,药物间相互作用少 在老年、肝肾功能受损等患者中应用均无需调整剂量
在老年、肝肾功能受损等患者中应用均无需调整剂量 可静脉-口服序贯给药
可静脉-口服序贯给药九、治疗效果评估
1.72小时评估
大多数CAP患者在初始治疗后72小时临床症状改善,但影像学改善滞后于临床症状应在初始治疗后72小时对病情进行评价,只要临床表现无恶化,可继续观察,不必急于更换抗感染药物(IA)2.初始治疗失败的危险因素

十、小结
CAP是全球发病和死亡的主要原因高危因素:高龄、共病、病毒感染、气道保护能力下降微生物:最常见是肺炎链球菌、G-菌、非典型病原体、厌氧菌等诊断三要素病情评估—治疗场所和预后病原体推断、耐药性预测和经验抗生素选择—最难—一个体化评估新型治疗药物奥马环素——抗菌谱广、安全、药物相互作用小、无肝肾功能影响、 可续贯口服来源:Dobutamine
