▎药明康德内容团队编辑
10月2日,诺贝尔生理学或医学奖授予mRNA疫苗的两位开发者——卡塔琳·卡里科(Katalin Karikó)博士和德鲁·魏斯曼(Drew Weissman)博士。
mRNA新冠疫苗的加速问世为人类带来了更多的健康保障,但这只是mRNA疫苗巨大潜能的冰山一角。除了在预防传染性疾病中的作用,mRNA疫苗还有着另一个诱人的应用场景:癌症疫苗。在这篇文章中,药明康德内容团队将与大家共同回顾mRNA疫苗的研发历程,以及在癌症治疗中的前景。

极具前景的想法
与我们熟悉的灭活病毒与减毒病毒不同,mRNA疫苗的思路是借助体外转录在体外合成mRNA,再将其递送至体内细胞,生产治疗或预防疾病所需的蛋白。但在上世纪80年代,受制于体外转录的mRNA的不稳定、递送的难度,以及体外生成的mRNA会在体内引起严重的免疫反应等障碍,mRNA技术并没有被看好。
卡里科和魏斯曼在科研上的交集始于1997年,当时两位任职于宾夕法尼亚大学的科学家在一台复印机旁聊了起来,卡里科研究的是mRNA的体外合成与注射至体内的技术,而师从著名传染病科学家Anthony Fauci博士的魏斯曼,研究方向则是树突状细胞——免疫反应中的重要抗原呈递细胞。当他们了解到彼此的研究方向与兴趣后,两人很快找到了共同的目标,那就是利用mRNA在体内合成目标蛋白,同时避免引起免疫反应。

▲德鲁·魏斯曼(Drew Weissman)博士和卡塔琳·卡里科(Katalin Karikó)博士(图片来源:Penn Medicine;摄影:Peggy Peterson)
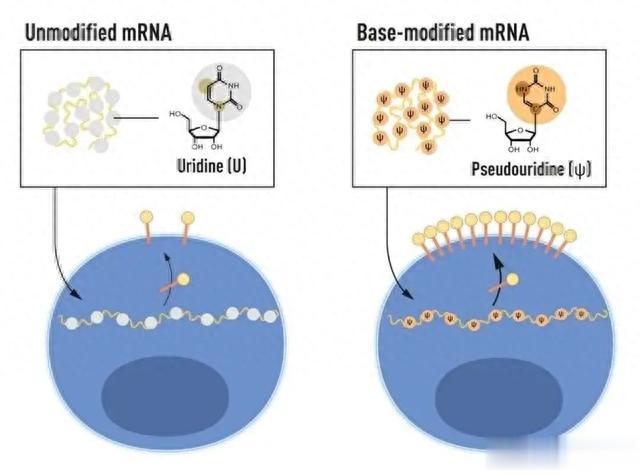
卡里科和魏斯曼注意到,树突状细胞将体外转录的mRNA识别为外来物质,从而激活并释放炎症信号分子。他们发现,体外转录的mRNA被识别,而哺乳动物的mRNA不会被识别的原因在于,哺乳动物细胞RNA中的碱基经常被化学修饰,体外转录的mRNA则没有。当他们产生不同的mRNA变体,每种变体都有特定的碱基修饰,这时体内不必要的炎症反应也几乎被清除了。
2005年,这项在今天看来意义重大的突破发表于《免疫学》(Immunity)杂志。在这项研究中,卡里科和魏斯曼不仅证实了碱基修饰的加入可避免体外转录mRNA可导致免疫激活,还揭示了含有假尿苷的 mRNA 能更高效地翻译,从而在接收了 mRNA 的细胞中产生更高的蛋白质产量。两位科学家与合作者还进一步证实,体外转录的mRNA会激活蛋白激酶R(PKR),这种抗病毒蛋白可以阻断蛋白翻译,保护细胞免遭入侵;而使用碱基修饰可降低PKR的激活,提高蛋白质产量。
此后他们又进一步发现,碱基修饰的mRNA既能减少炎症反应,也能增加蛋白质产量。卡里科和魏斯曼清除了mRNA应用道路上的关键障碍。
▲碱基修饰的体外转录mRNA 具有更高的蛋白表达(图片来源:诺贝尔奖官网;The Nobel Committee for Physiology or Medicine. Ill. Mattias Karlén)
“20年来,在任何人了解、关注我们之前,我们一直在并肩工作。”魏斯曼说,由于他和卡里科都有睡眠障碍,因此他们经常会在凌晨三五点发邮件来交流新想法。基于这样紧密的合作关系,两位科学家在不被看好的情况下改变了疾病治疗与预防的格局。
随着技术的成熟,人们对mRNA疫苗展现出更浓厚的兴趣。多家生物技术公司开始了基于mRNA技术的研发,而传染性疾病与癌症,成为了最受关注的两大热点方向。
癌症治疗前景
肿瘤细胞的突变会产生新抗原,由于这些新抗原通常只存在于肿瘤细胞内,因此它们成为了开发癌症疫苗的有效靶点。mRNA治疗癌症的基本原理是,mRNA进入细胞后可以翻译生成新抗原蛋白,利用新抗原激活B细胞和T细胞的免疫应答,从而增强对抗癌症的能力。
由于不同患者的肿瘤具有各自独特的抗原特征,因此基于这一特征的个体化癌症疫苗成为重点研发方向。研究人员从患者身上采集组织样本,利用基因组测序等手段从患者的肿瘤细胞中找到新抗原,并且根据新抗原序列合成mRNA,作为疫苗注射至患者体内。这些疫苗可以特异性靶向多种新抗原,激发对肿瘤细胞的免疫反应。

图片来源:123RF
目前,数十项临床试验正在检验mRNA疫苗对胰腺癌、结直肠癌、黑色素瘤等多种癌症的安全性与有效性,此外一些试验将mRNA疫苗与增强人体对肿瘤免疫反应的药物相结合,以评估疗效。
例如在2021年的一篇《科学-转化医学》论文中,一款mRNA疫苗就在小鼠实验中缩小了肿瘤体积,并且延长了生存期。目前,针对该疫苗与帕博利珠单抗联合治疗头颈部鳞状细胞癌的临床试验正在进行。此后,多款全新的mRNA疫苗在小鼠实验中成功清除了HPV感染相关的肿瘤,使得大多数小鼠在实验结束时都处于无癌状态。
今年,《自然》杂志的一项重磅研究更是向致命的“癌症之王”胰腺癌发起了挑战。胰腺癌的新抗原表达水平很低,因此目前的免疫检查点抑制剂(ICI)对胰腺癌的疗效极为有限。在这项1期临床试验中,研究团队设计了可编码数十种新抗原的mRNA疫苗,以增强胰腺癌患者免疫系统对新抗原的反应,让T细胞更容易击杀癌细胞。患者在接受免疫疗法与化疗联合治疗的同时,注射了mRNA癌症疫苗,结果大约有一半的患者会对癌症疫苗产生有效的免疫反应,并且在18个月的随访期没有复发。由此,试验证实了mRNA疫苗在治疗难治性癌症中的巨大潜力。

▲针对胰腺癌的癌症疫苗策略(图片来源:参考资料[5])
我们看到,基于mRNA的个体化癌症疫苗正在临床或临床前试验中显示出令人欣喜的疗效,癌症治疗有望迎来新的格局。但需要指出的是,目前尚未有mRNA癌症疫苗获批上市,这些疫苗也存在一些有待克服的难题。无论是mRNA作为外源物质的免疫原性,对不断突变的癌细胞新抗原的识别能力,还是递送问题中的挑战,都需要全球研发人员持续探索基础机制、优化研发流程。我们期待,从卡里科和魏斯曼实验室中走出的科学突破,将在不久的未来造福全球更多癌症、传染性疾病患者。
